




前部分内容已对药物合成路线的设计、选择,反应条件的优化,中间体、目标产物的质量控制及后处理方法等内容进行了系统的介绍,现结合塞来昔布的生产工艺说明上述几方面在药物合成工艺研究中的重要作用。
塞来昔布(celecoxib,4-111),中文化学名称为4-[3-(三氟甲基)-5-(4-甲基苯基)-1 H -吡唑-1-基]苯磺酰胺,英文名称为4-[5-(4-methylphenyl)-3-(trifluoromethyl)-1 H -pyrazol-1-yl]ben-zenesulfonamide,结构如图4-47,于1999年1月在美国首次上市的第一个环氧合酶-2(COX-2)选择性抑制剂,通过阻止炎性前列腺素类物质(前列腺素E 1 、前列腺素D 2 及前列环素等)的产生,达到抗炎、镇痛及退热作用,其商品名为celebrex。临床上它主要用于缓解骨性关节炎、类风湿性关节炎的症状和体征,也适用于强直性脊柱炎、原发性痛经、急性疼痛等,还可减少家族性腺瘤息肉患者腺瘤性结直肠息肉量。
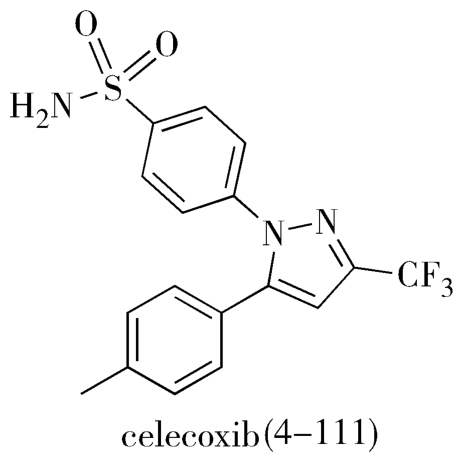
图4-47 塞来昔布(celecoxib)的结构式
对塞来昔布的结构式进行逆合成分析,如图4-48所示,吡唑环为拆键部分,可由对氨磺酰基苯肼盐酸盐(4-112)和1-(4-甲基苯基)-4,4,4-三氟丁烷-1,3-二酮(4-113)环合而成。1-(4-甲基苯基)-4,4,4-三氟丁烷-1,3-二酮(4-113)可在碱的催化作用下,由对甲基苯乙酮与三氟乙酸酯经Claisen缩合而成,对甲基苯乙酮可由甲苯经傅-克酰基化反应制得。
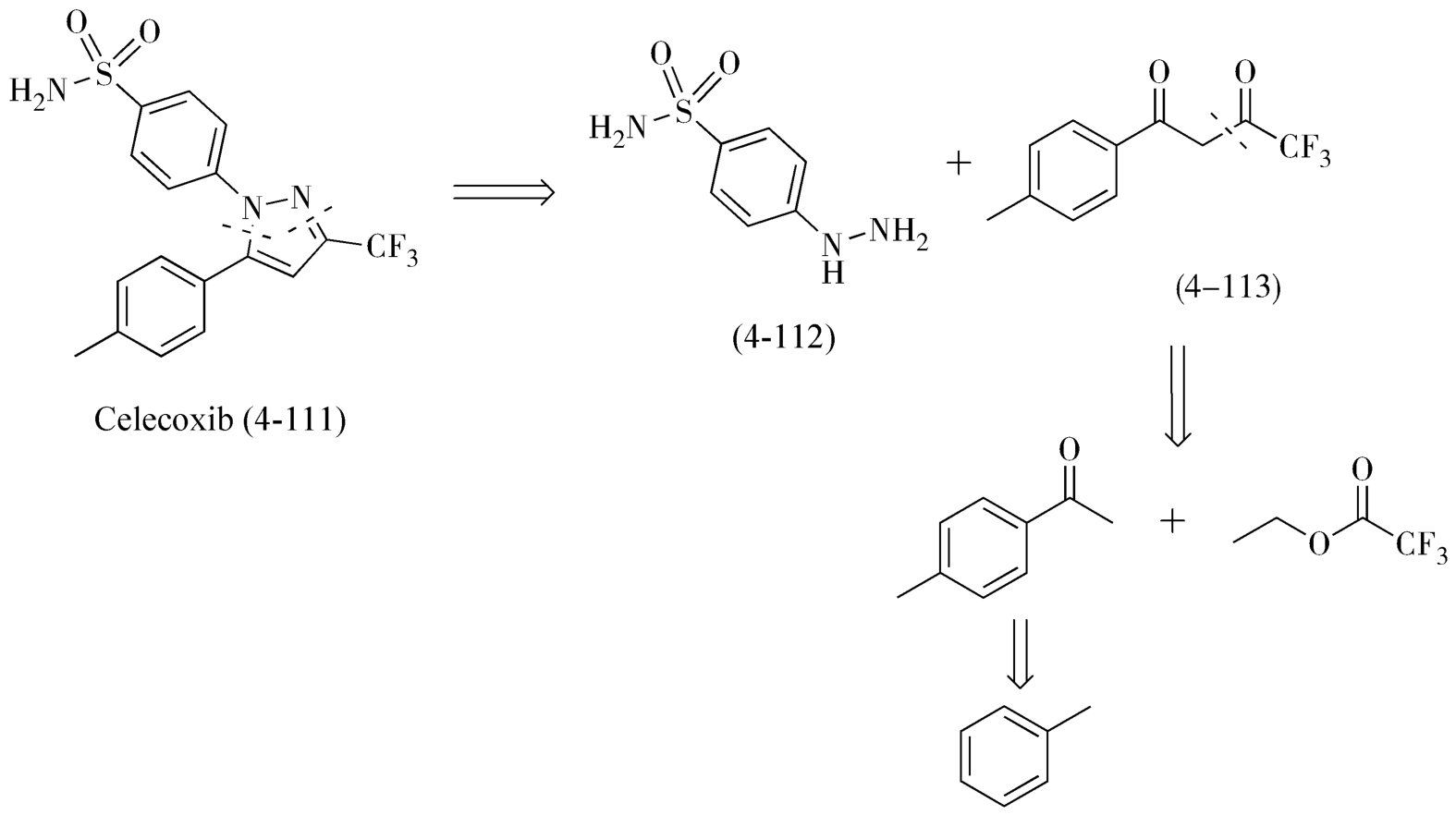
图4-48 塞来昔布的逆合成分析
1.1-(4-甲基苯基)-4,4,4-三氟丁烷-1,3-二酮(4-113)的合成 甲苯在三氯化铝的作用下与乙酸酐或乙酰氯进行傅-克酰基化反应得到对甲基苯乙酮,它与三氟乙酸乙酯或三氟乙酸β-三氟乙酯缩合得到目标产物,如图4-49所示。其中,对甲基苯乙酮与三氟乙酸 β -三氟乙酯在六甲基乙硅叠氮锂的作用下缩合得到目标产物,收率为86%,该法所用试剂较贵;而对甲基苯乙酮与三氟乙酸乙酯在甲醇钠的作用下发生缩合反应的收率为94%,此路线原料廉价易得,收率高于前一方法。
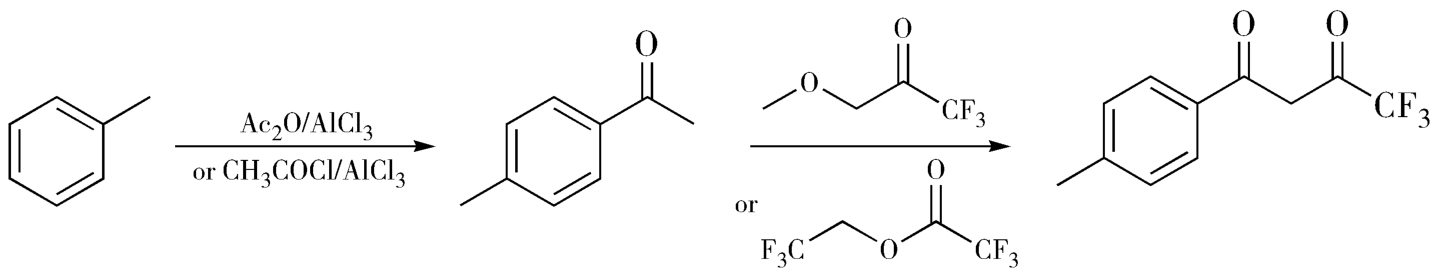
图4-49 1-(4-甲基苯基)-4,4,4-三氟丁烷-1,3-二酮的合成
2.塞来昔布的合成 塞来昔布是由对氨磺酰基苯肼(4-112)盐酸盐和1-(4-甲基苯基)-4,4,4-三氟丁烷-1,3-二酮(4-113)环合而成的,环合条件的不同之处主要是所用溶剂的不同。
(1)以1,3-二甲基-3,4,5,6-四氢-2(1H)-嘧啶酮(DMPU)为溶剂 对氨磺酰基苯肼(4-112)盐酸盐和1-(4-甲基苯基)-4,4,4-三氟丁烷-1,3-二酮(4-113)在DMPU中,6mol/L盐酸催化下,室温搅拌16小时,HPLC检测塞来昔布的异构体(4-114)的含量只有0.16%,含一分子DMPU的塞来昔布结晶体(4-115)的收率为83%,如图4-50所示。
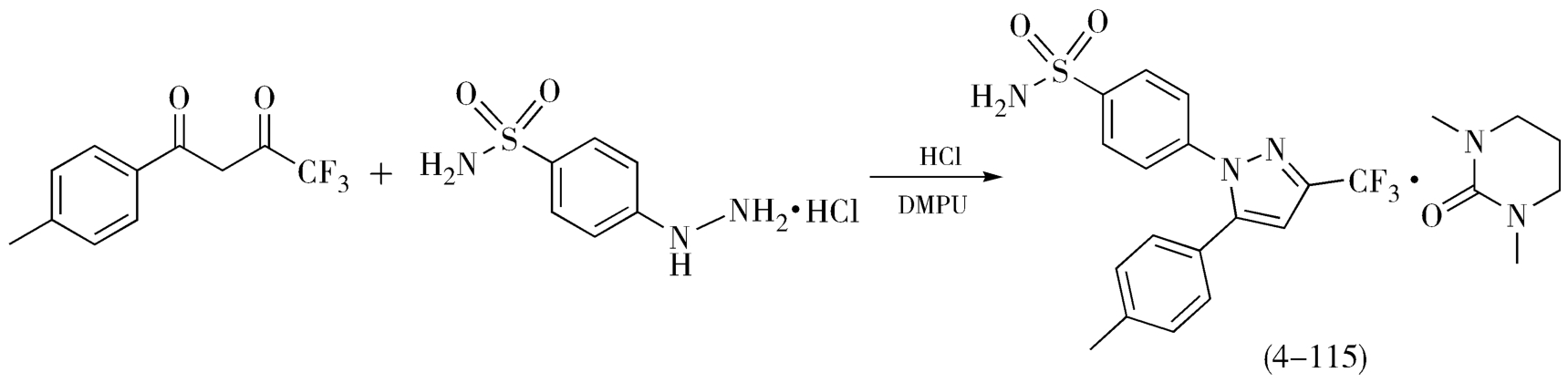
图4-50 塞来昔布的合成(DMPU为溶剂)
(2)以 N -甲基-2-吡咯烷酮为溶剂 以 N -甲基-2-吡咯烷酮(NMP)为溶剂,6mol/L盐酸的催化作用下,对氨磺酰基苯肼盐酸盐和1-(4-甲基苯基)-4,4,4-三氟丁烷-1,3-二酮环合反应16小时,得到含一分子NMP结晶的塞来昔布(4-116),如图4-51,收率为85%,HPLC检测其异构体(4-114)含量为0.03%。
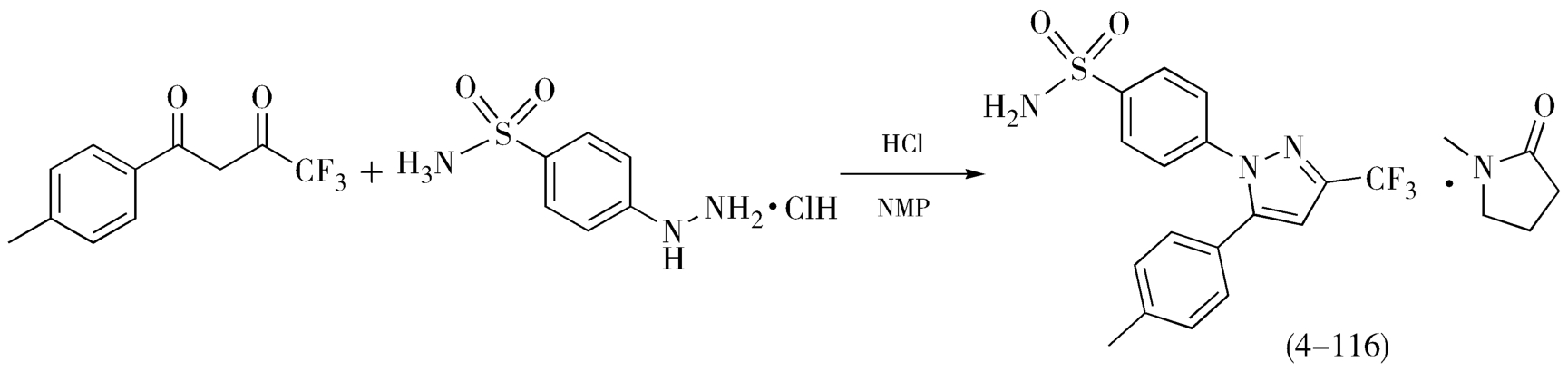
图4-51 塞来昔布的合成(NMP为溶剂)
上述两种方法反应条件温和,产品纯度及收率较高,但酰胺类溶剂用量较大,成本较高。故工业上生产塞来昔布并未采用以上两种方法,而是以醇类作为溶剂进行环合制备的,如图4-52。
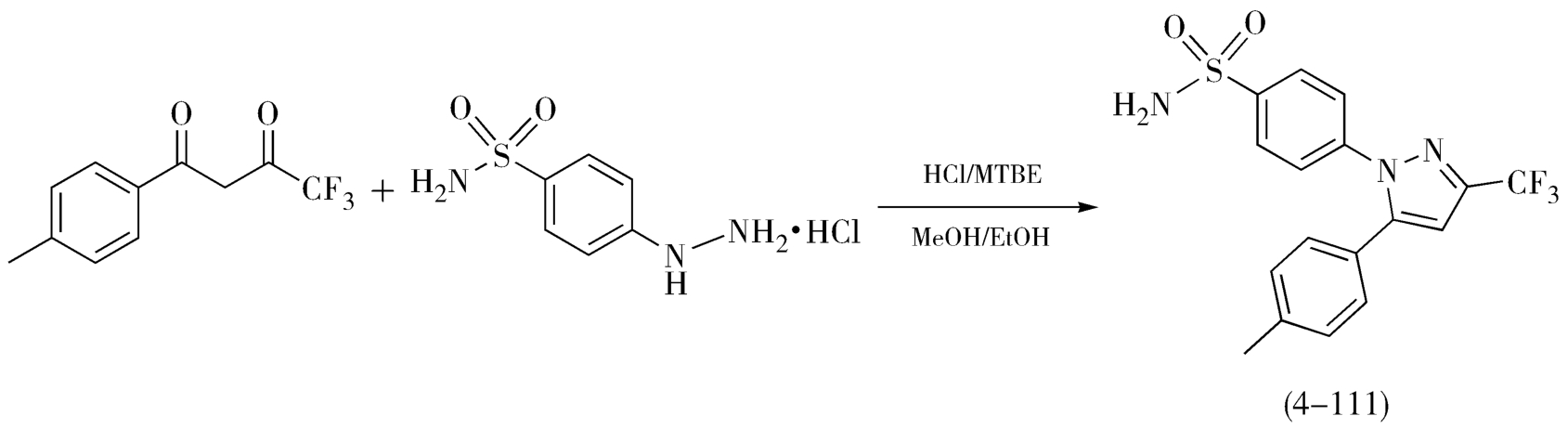
图4-52 塞来昔布的合成(醇为溶剂)
经上述合成路线的选择,最终确定了适合于工业生产的塞来昔布的合成路线,具体如图4-53所示:
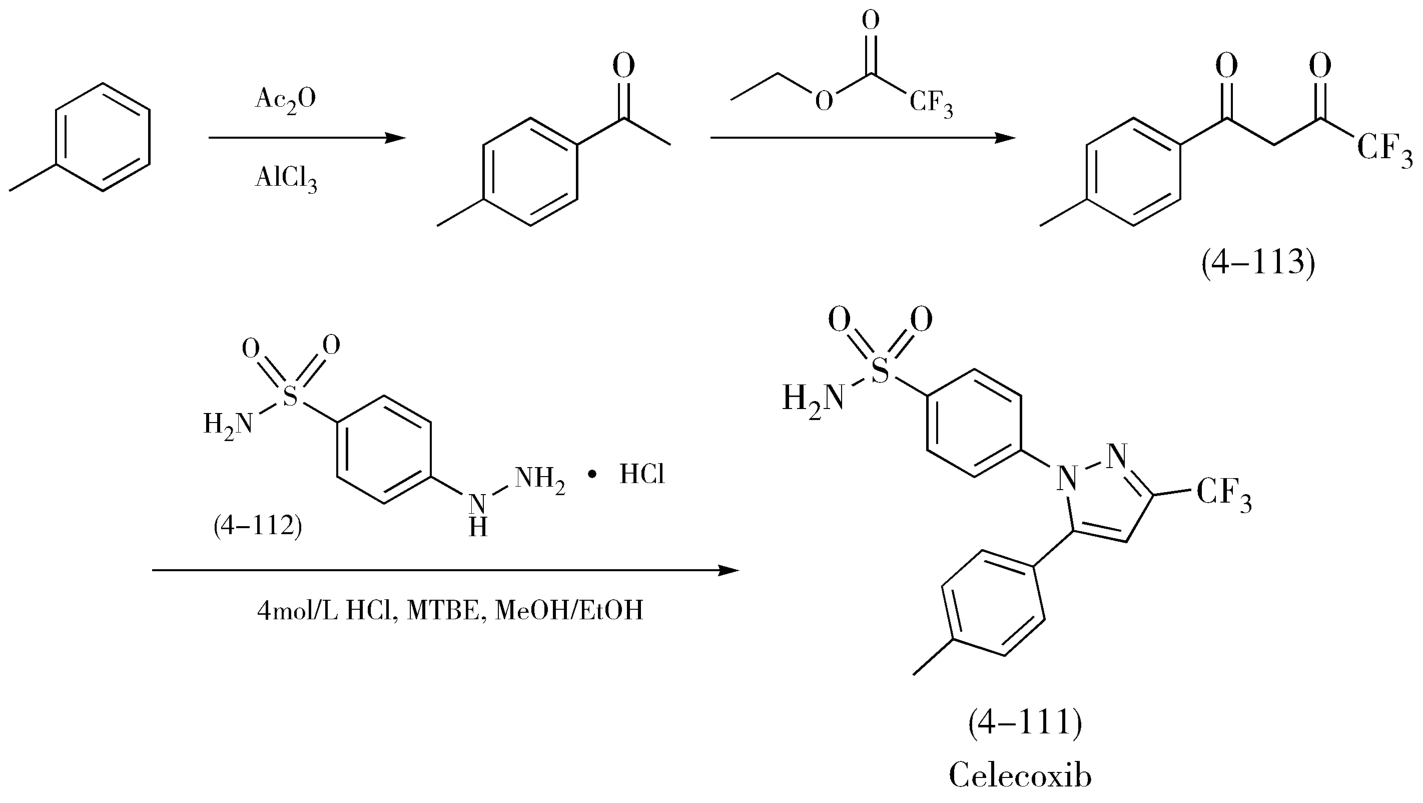
图4-53 塞来昔布的合成路线
下面将对其工艺原理和过程进行讨论:
(1)工艺原理 甲苯与醋酐在无水三氯化铝的作用下,经乙酰化得对甲基苯乙酮。醋酐在路易斯酸的催化下,形成酰基正离子,与苯环发生亲电取代反应,进攻甲基的邻对位,如图4-54所示。
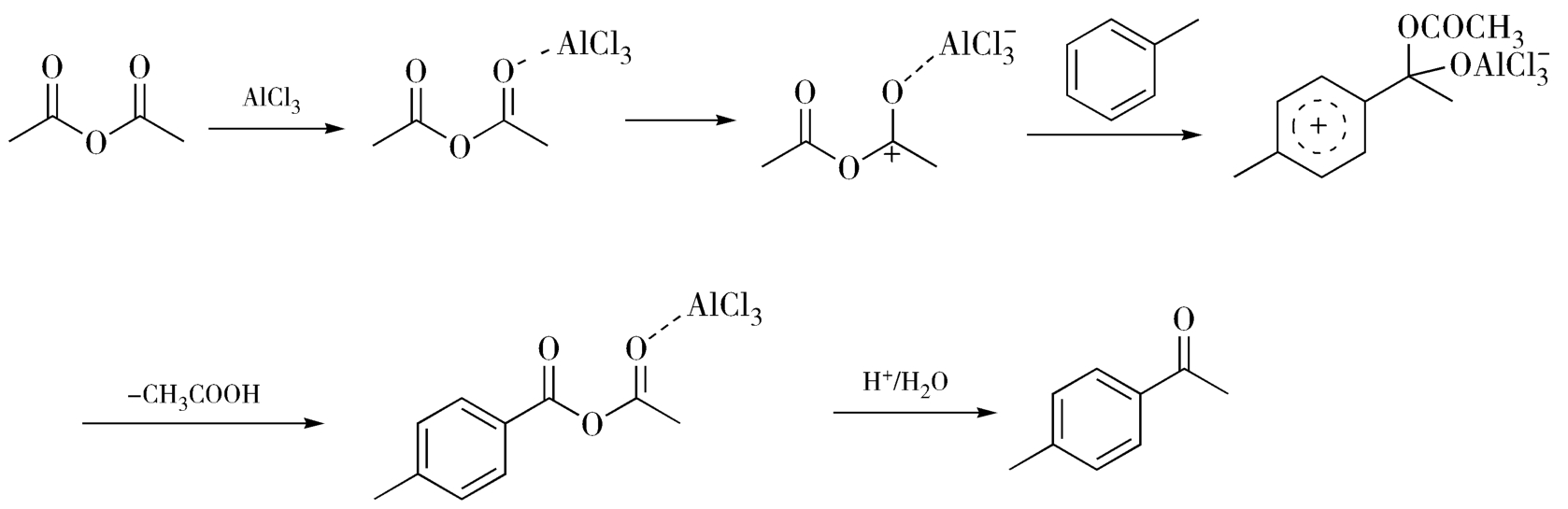
图4-54 以甲苯和醋酐为原料合成对甲基苯乙酮的工艺原理示意图
(2)工艺过程 将干燥的甲苯和无水三氯化铝粉末加入至反应瓶内,搅拌下滴加醋酐,温度逐渐升至90℃,有大量氯化氢气体放出。反应至不再产生氯化氢气体,冷却至室温,将反应液倒入碎冰和浓盐酸的混合物中,搅拌至铝盐全部溶解为止。分离出有机层,水洗,10%氢氧化钠水溶液洗至碱性,再用水洗至中性。干燥后,减压蒸馏,收集93~94℃/7mmHg的馏分,得对甲基苯乙酮,收率为86%。
(3)反应条件及影响因素
1)甲苯的傅-克酰基化可发生在甲基的对位,也可发生在邻位。由于邻位的空间位阻效应,乙酰化优先发生在对位。如果温度过高,会增加邻位乙酰化副产物的生成量。
2)催化剂的作用在于增强乙酰基碳原子的电正性,增强其亲电能力。此类反应中,路易斯酸的催化能力强于质子酸。常用的路易斯酸有AlCl 3 、BF 3 、SnCl 4 、ZnCl 2 等。其中,AlCl 3 廉价易得且能溶于有机溶剂,正因为如此,它较为常用于此类反应中。
3)傅-克酰基化反应常用溶剂有二硫化碳、硝基苯、石油醚、四氯乙烷、二氯乙烷等。其中,硝基苯与AlCl 3 可形成复合物,反应呈均相,应用较广。在甲苯的乙酰化反应中,过量的甲苯兼作溶剂。
(1)工艺原理 对甲基苯乙酮在甲醇钠的作用下生成碳负离子,它与三氟乙酸乙酯发生亲核加成-消除反应,得到目标产物(4-113)。
(2)工艺过程 在氩气保护下,将对甲基苯乙酮溶于甲醇中并加入25%甲醇钠的甲醇溶液,搅拌5分钟,加入三氟乙酸乙酯,加毕,回流24小时。将反应液冷却至室温,浓缩,加入100mL 10%的盐酸,乙酸乙酯萃取,有机相干燥,浓缩得油状物,收率为94%。产物无需进一步纯化,可直接用于后续反应。
(3)反应条件及影响因素 对甲基苯乙酮的 α -氢活性较小,在甲醇钠作用下缩合效果较好。甲醇钠与对甲基苯乙酮的摩尔比约为1∶1.1,反应需在无水条件下进行。
(1)工艺原理 对氨磺酰基苯肼盐酸盐与1-(4-甲基苯基)-4,4,4-三氟丁烷-1,3-二酮(4-113)发生亲核加成-消除反应,环合得到塞来昔布。对氨磺酰基苯肼(4-114)盐酸盐中肼基的 β -氮原子(末端氮原子)上的未共用电子对进攻原料(4-113)的3-位羰基碳原子,脱去1分子水形成碳氮双键,得到中间体(4-115),其肼基中 α -氮原子的未共用电子对再进攻1-位羰基碳原子,形成五元环,再脱去一分子水后得到吡唑衍生物塞来昔布,见图4-55。
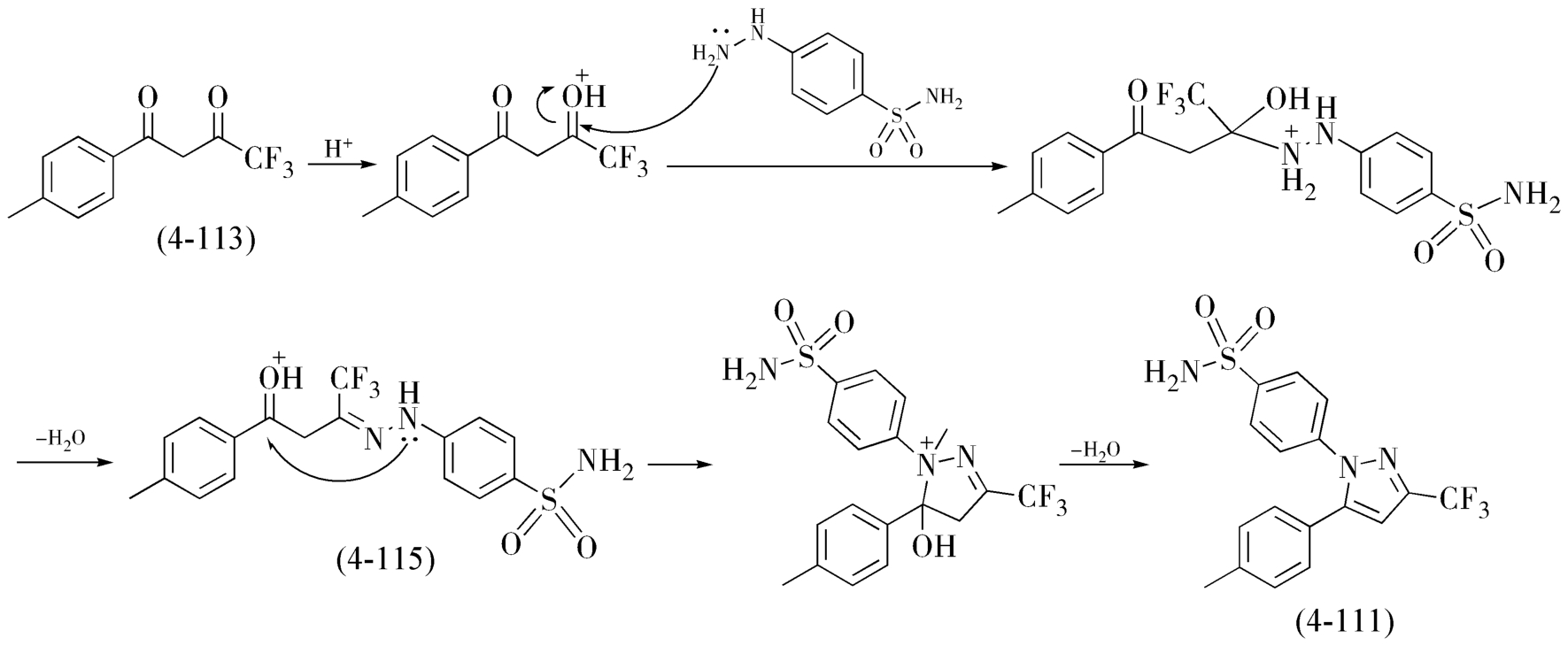
图4-55 塞来昔布的合成工艺原理示意图
(2)工艺过程 等摩尔比的对氨磺酰基苯肼盐酸盐与1-(4-甲基苯基)-4,4,4-三氟丁烷-1,3-二酮混合后,再加入乙醇、甲基叔丁基醚(MTBE)、甲醇和等摩尔的4mol/L盐酸,加毕,回流3小时。冷却,减压浓缩,滴加水后产物结晶析出。室温静置1小时后,过滤,分别用60%乙醇和水洗涤,干燥得目标产物塞来昔布,收率为76.4%。
(3)反应条件及影响因素 对氨磺酰基苯肼盐酸盐与1-(4-甲基苯基)-4,4,4-三氟丁烷-1,3-二酮(4-113)的环合需要酸来催化。后者的结构中与三氟甲基相连的3-位羰基的亲电活性大于与苯基相连的1-位羰基,作为催化剂的稀酸优先使3-位羰基活化,降低了活化能,缩短了反应历程,同时提高了反应的区域选择性,使生成目标产物塞来昔布的量远远多于异构体(4-114)的量。生成异构体的反应历程可能有如下两种,见图4-56反应历程Ⅰ,图4-57反应历程Ⅱ。
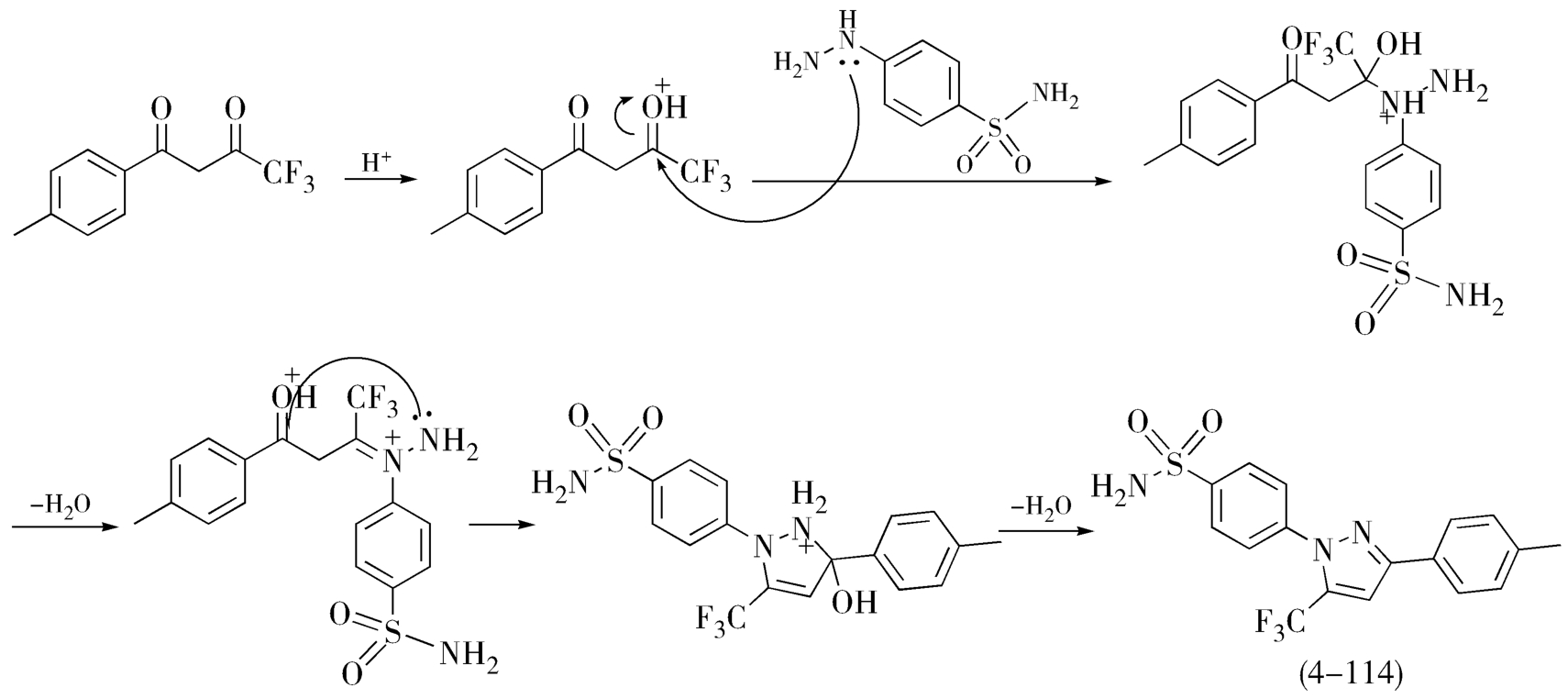
图4-56 反应历程Ⅰ示意图
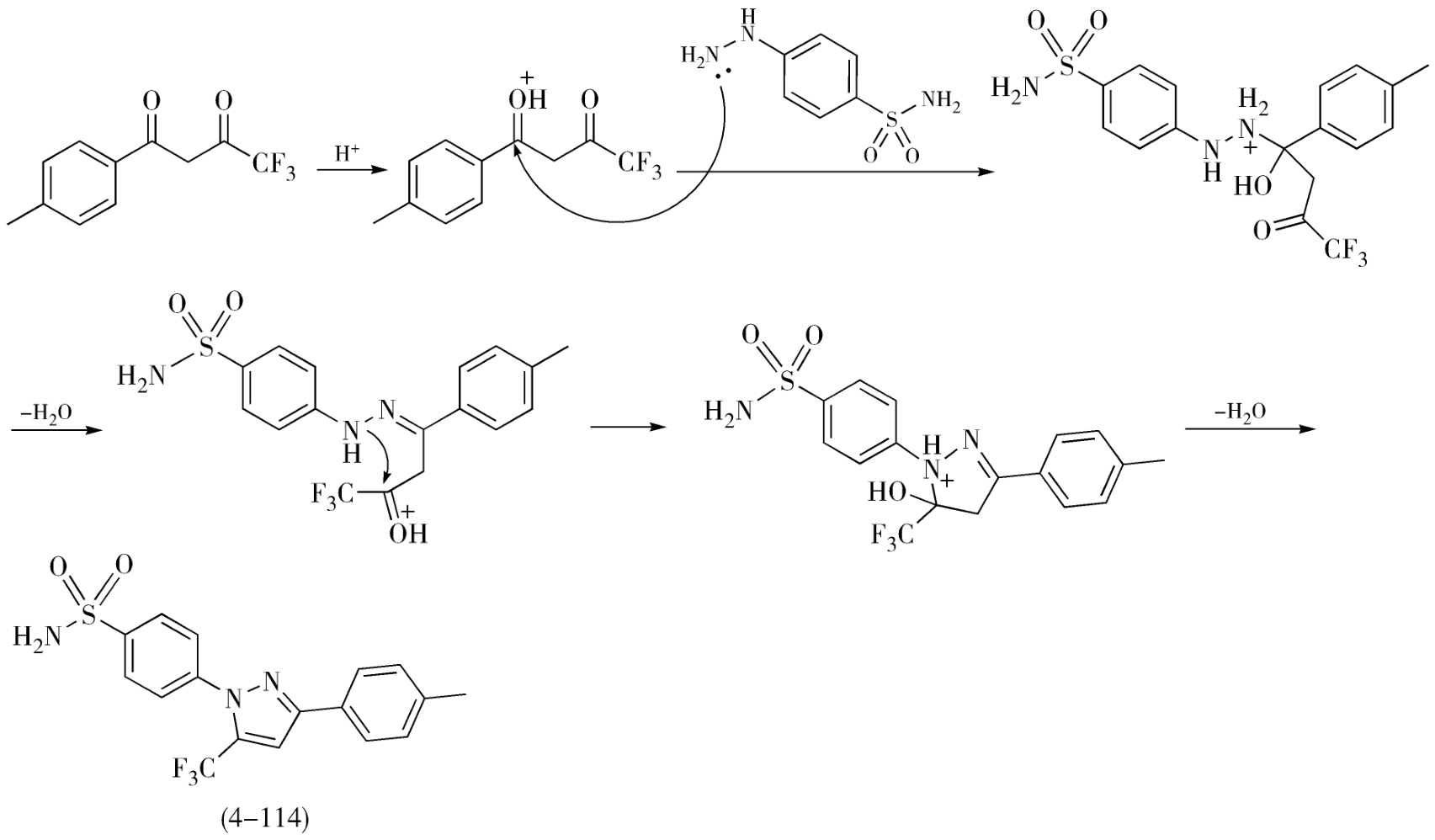
图4-57 反应历程Ⅱ示意图