




抗菌增效剂甲氧苄啶(trimethoprim,TMP,4-1)能够抑制细菌二氢叶酸还原酶,阻止细菌核酸合成,主要用作磺胺类抗菌药物的增效剂。它与磺胺甲
 唑(sulfamethoxazole,SMZ)组成的复方片剂(1∶5)称为复方新诺明,与磺胺嘧啶(sulfadiazine,SD)合用(1∶10)组成的双嘧啶片都是国内目前应用很广的抗菌制剂,但在欧美一些经济发达国家,甲氧苄啶作为牲畜用药远远大于人用临床。
唑(sulfamethoxazole,SMZ)组成的复方片剂(1∶5)称为复方新诺明,与磺胺嘧啶(sulfadiazine,SD)合用(1∶10)组成的双嘧啶片都是国内目前应用很广的抗菌制剂,但在欧美一些经济发达国家,甲氧苄啶作为牲畜用药远远大于人用临床。
甲氧苄啶最早由Hitchings等人于1959年合成成功,1962年Stenbuck等人应用于工业生产,目前全世界有几十个国家生产。在我国,甲氧苄啶生产企业最多时达到40多家,1997年年产量曾达1737吨。甲氧苄啶的合成剖析思路如下(图4-1)。
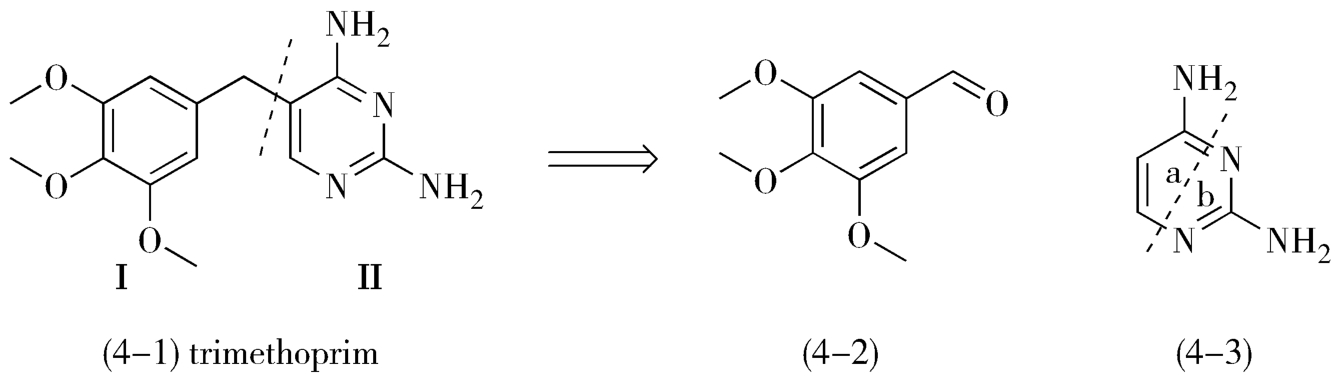
图4-1 甲氧苄啶的合成剖析思路
从甲氧苄啶化学结构考察,可将其分为Ⅰ和Ⅱ两部分。Ⅰ部分是合成甲氧苄啶的重要中间体,它的化学结构应具有形成C-C的活性功能基,目前应用最多的是3,4,5-三甲氧基苯甲醛(4-2);Ⅱ部分为2,4-二氨基嘧啶衍生物,若先合成2,4-二氨基嘧啶(4-3)再与Ⅰ部分缩合,则由于嘧啶环上的氨基须先加以保护和在5位引入基团的困难,使工艺路线冗长。所以在生产过程中采用逐步形成嘧啶环的途径,即将嘧啶开剖析成a和b两部分,将Ⅰ部分与a部分首先缩合,最后与b部分环合(图4-2)。
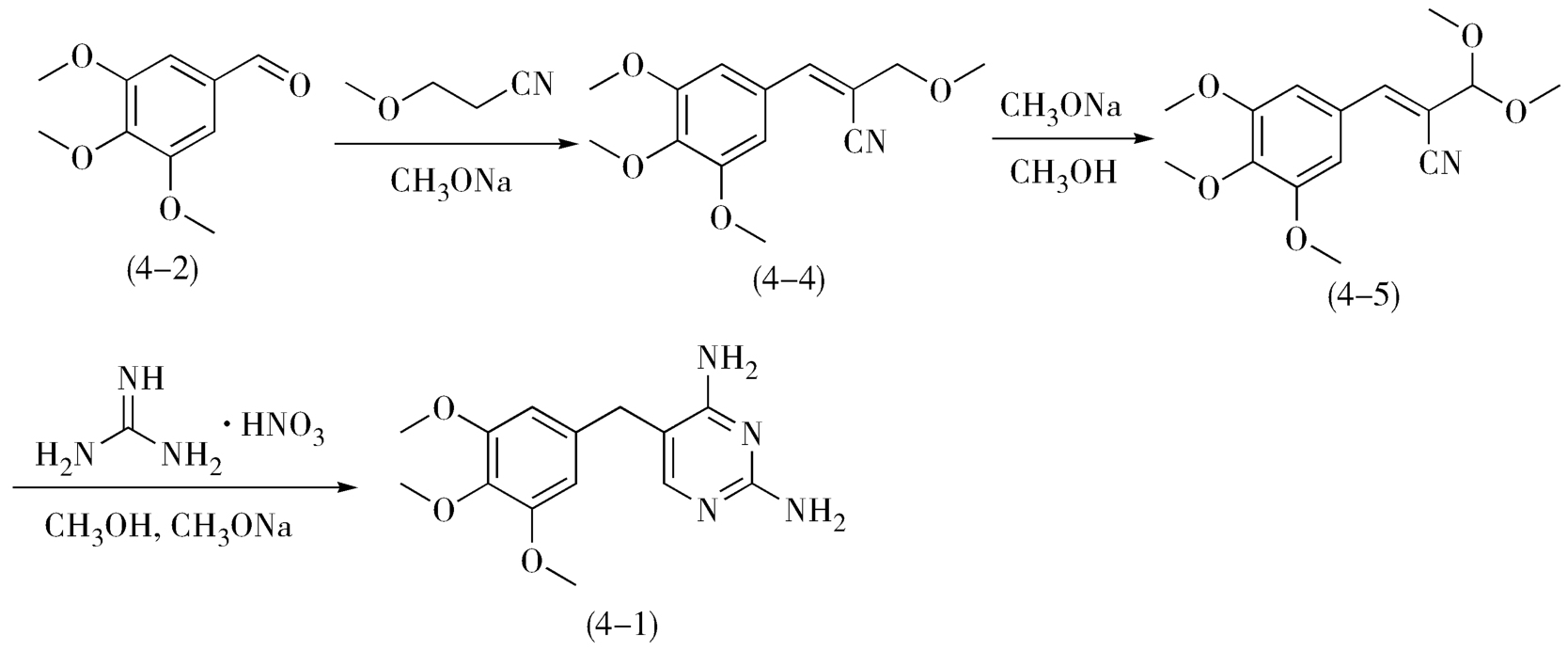
图4-2 甲氧苄啶的合成反应
关键中间体3,4,5-三甲氧基苯甲醛(4-2)的合成按原料来源与化学反应中功能基的转化又可分为以下几条途径。
20世纪80年代,我国的甲氧苄啶生产主要以没食子酸(4-6)为原料(图4-3)。
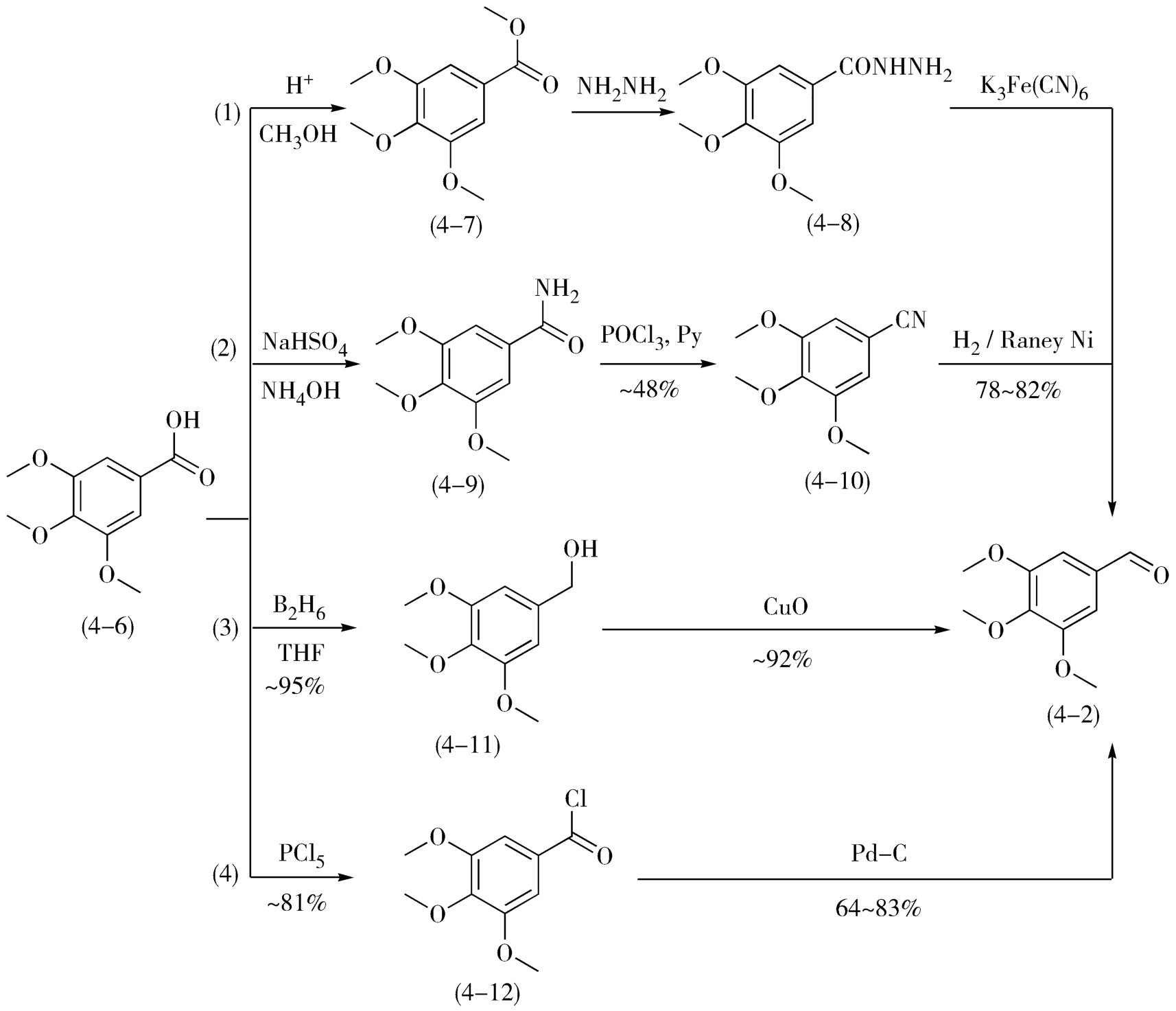
图4-3 以没食子酸为原料合成3,4,5-三甲氧基苯甲醛示意图
在以没食子酸为原料的几条路线中,第(2)(3)(4)三条路线需用价格较为昂贵的硼烷或贵金属催化剂,有的还需使用三氯氧磷,存在劳动保护和腐蚀设备的问题,因此虽然收率较高,但在生产过程中并未大规模应用。相比之下,第(1)条路线工艺条件简易,收率较高,试剂价格便宜,因此得到大规模应用。
没食子酸系由五倍子中的鞣酸水解制取。五倍子本身是一种重要的中药材,大部分供直接出口,因此用它来制取没食子酸的数量有限。这样不仅使甲氧苄啶的价格昂贵,也使各生产企业为原料来源大伤脑筋,生产能力受限,规模偏小。于是到20世纪80年代中后期,国内外的甲氧苄啶生产企业纷纷投入人力、物力研究开发甲氧苄啶的新合成路线。到了20世纪90年代,由于3,4,5-三甲氧基苯甲醛的生产工艺日臻成熟及化工原料价格的不断下调,使3,4,5-三甲氧基苯甲醛的价格已低于五倍子。
香兰醛(4-13)的来源有天然和人工合成两种途径。天然来源是从木材造纸废液中回收得木质磺酸钠,再经氧化得香兰素醛。香兰醛在木质磺酸钠中含量约占15%,因此资源丰富,价格便宜,值得在化学制药工业上广为利用;另一条来源是以邻氨基苯甲醚(4-14)为原料,经愈创木酚(4-15)和引入醛基而得到香兰醛(4-13)。香兰醛再经溴化、水解得5-羟基香兰醛(4-17),再甲基化可得3,4,5-三甲氧基苯甲醛(4-2),三步总产率74.5%。这是目前制备3,4,5-三甲氧基苯甲醛的方法中反应步骤最短、收率较高的路线,已应用于生产(图4-4)。
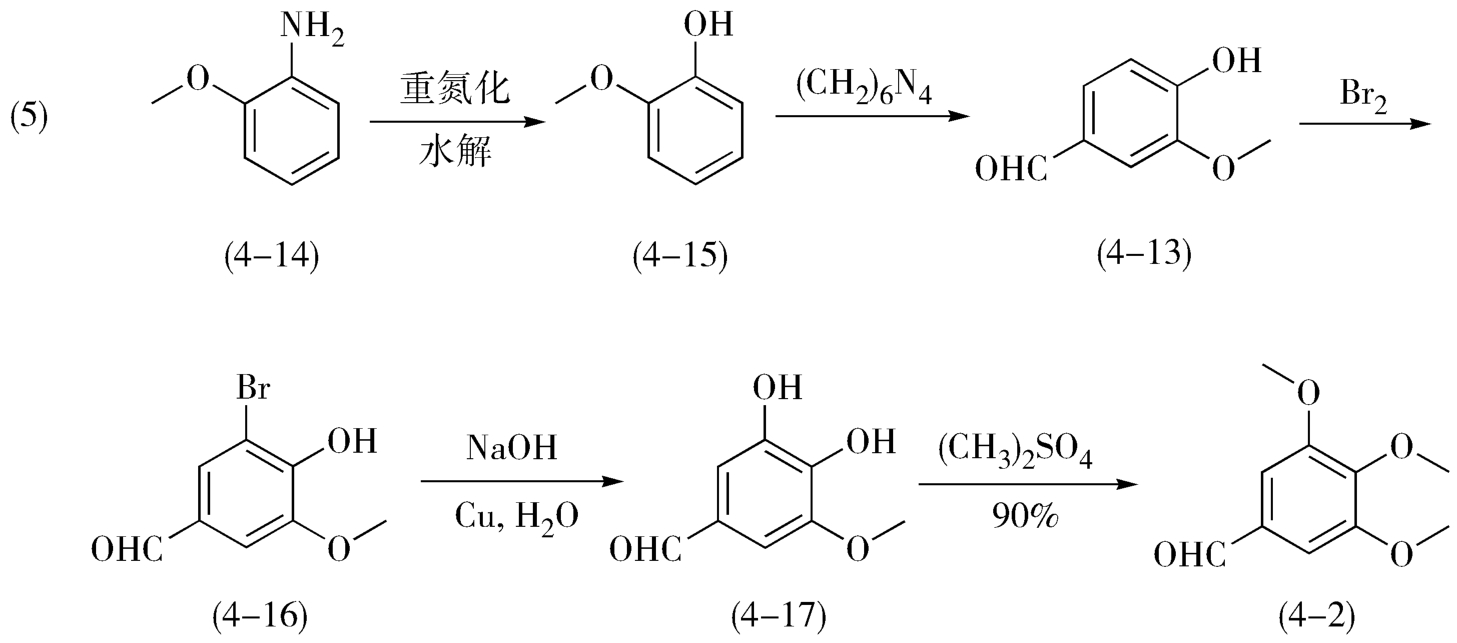
图4-4 以香兰醛为原料合成3,4,5-三甲氧基苯甲醛示意图
对硝基甲苯(4-18)在多硫化钠醇碱溶液作用下,经氧化、还原反应制得对氨基苯甲醛(4-20),对氨基苯甲醛经重氮化、水解制得对羟基苯甲醛(4-21),再经溴化、甲氧基化、甲基化得到3,4,5-三甲氧基苯甲醛(4-2),总收率20%左右(图4-5)。
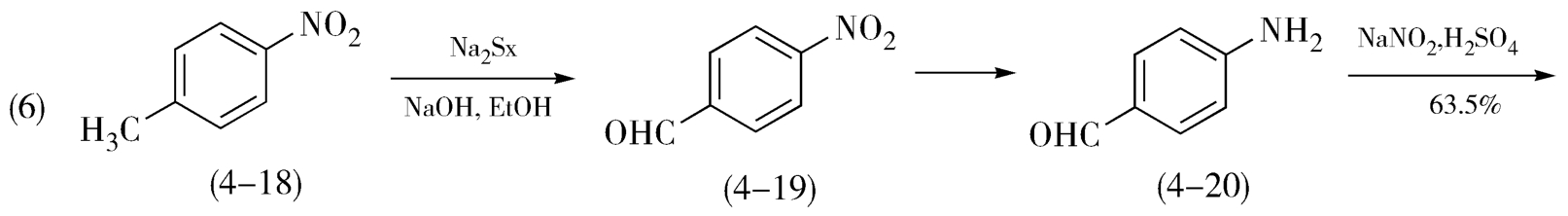
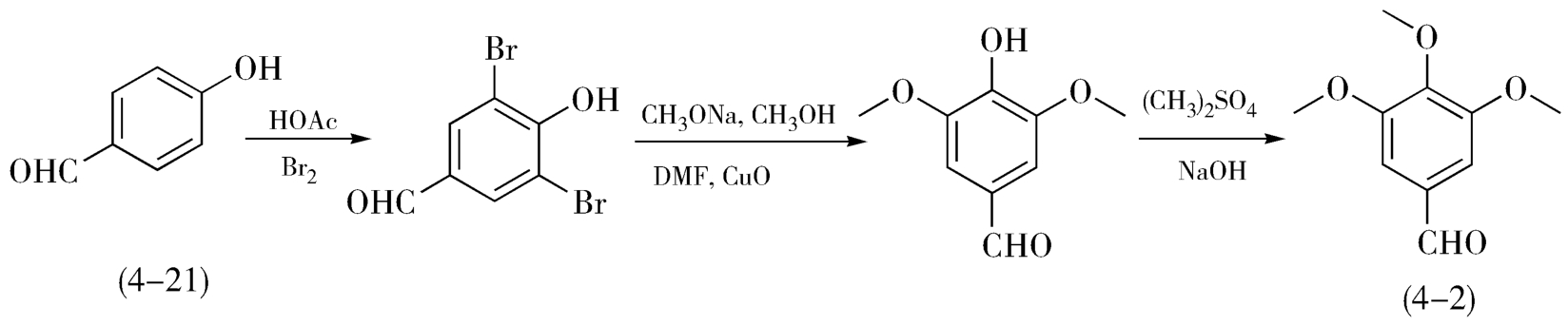
图4-5 以对硝基甲苯为原料合成3,4,5-三甲氧基苯甲醛示意图
对硝基甲苯来源广泛,价格低廉,因此,此条合成路线具有较大的应用价值。但此条工艺路线中需要使用大量溴素,如何保证溴素供应和做好劳动保护是需要注意的问题。此外,在制备对羟基苯甲醛(4-21)时反应液体积大、耗气量多等问题也需要很好地解决。
从苯酚(4-22)合成3,4,5-三甲氧基苯甲醛(4-2)关键在于如何导入醛基。先导入醛基会产生少量邻位副产物,收率较低,所得产物对羟基苯甲醛(4-21)易于聚合,产生大量树脂,需要处理,且反应时间需20余小时,生产周期较长。从对羟基苯甲醛到3,4,5-三甲氧基苯甲醛(4-2)的合成方法与前面路线一致,总收率20%左右(图4-6)。
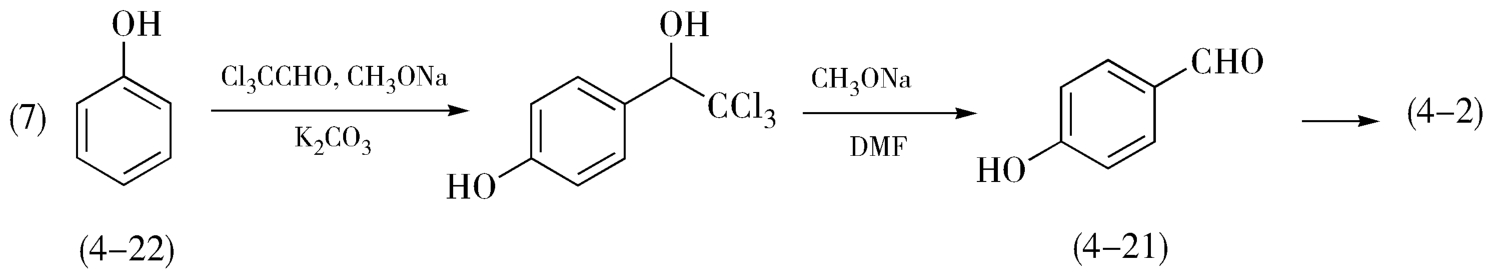
图4-6 以苯酚为原料合成3,4,5-三甲氧基苯甲醛
针对上述合成路线的缺点,可以考虑先上溴,再导入醛基。由于羟基为邻对位取代基,因此必须首先将羟基的对位进行保护,使溴代反应仅在邻位进行,制得2,6-二溴苯酚(6-23),再进行甲氧基置换反应,最后导入醛基(图4-7)。
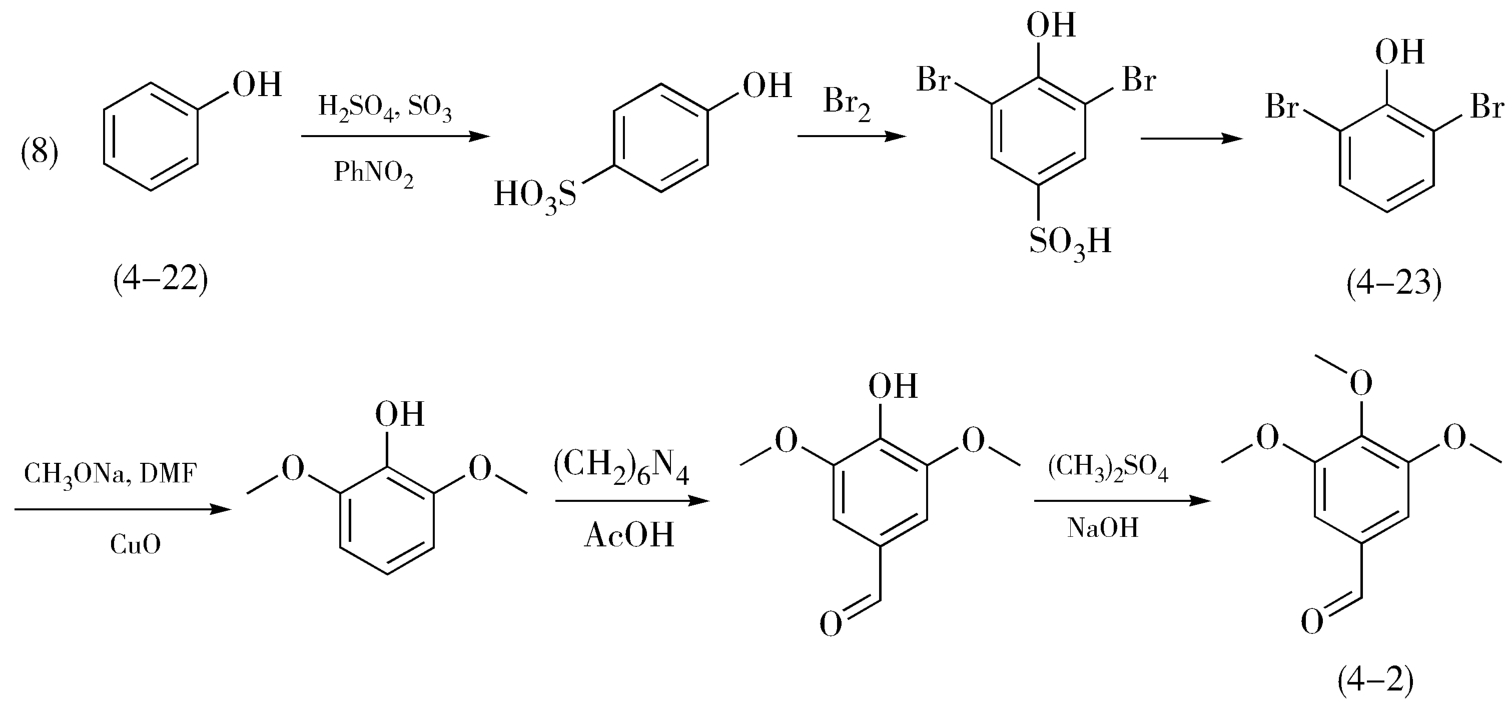
图4-7 以苯酚为原料合成3,4,5-三甲氧基苯甲醛的改进方法
生产中首先使用磺酸基对苯酚对位进行保护,然后在苯酚的磺化液中直接加入溴生成二溴化物。反应液可不经分离直接进行过热水蒸气蒸馏,在蒸馏过程中进行水解,消除对位磺酸基生成2,6-二溴酚(4-23)。以上三步反应实际是一个工序,在同一反应釜中完成,即所谓的连续反应;然后甲氧基化、导入醛基制得丁香醛,最后甲基化得到3,4,5-三甲氧基苯甲醛,总收率35%。
对甲酚(4-24)经磺化、水解、甲基化和氧化反应步骤可制得3,4,5-三甲氧基苯甲醛(图4-8)。
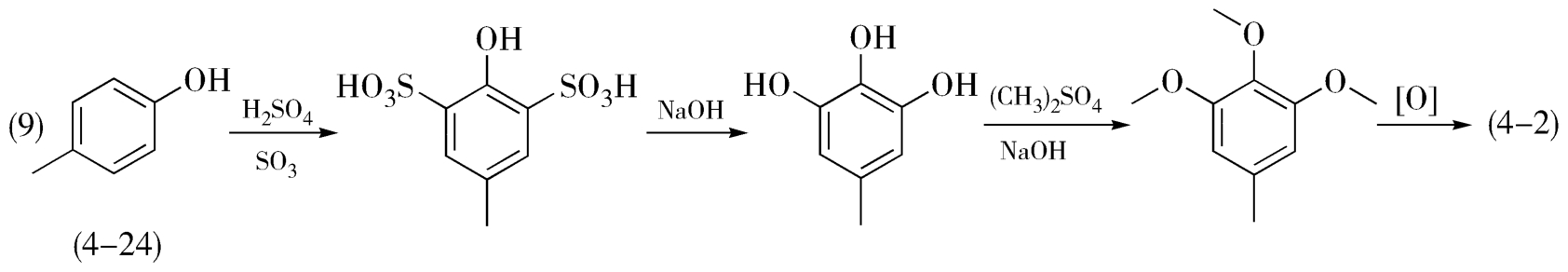
图4-8 以对苯酚为原料合成3,4,5-三甲氧基苯甲醛反应
对甲酚由炼焦的副产品粗甲酚经分馏制得,但一般分馏所得为间位和对位甲酚的混合物,二者沸点相差仅0.5℃,需采用特殊方法分离,增加成本,成为此条合成路线的最大缺点。
综合考察各条生产路线,第(6)条至第(9)条生产路线均以基本化工原料为起始原料,价格便宜,来源有保障,但第(8)条生产路线比第(7)条生产路线具有明显优势,其他各条路线由于起始原料不同,则应从经济效益、社会效益、生产难度、前期投入等多方面加以考虑,结合生产企业自身情况,认真选择。值得一提的是,如果原料来源有保障,第(5)条生产路线也许会比其他各条生产路线具有更大的合理性。
布洛芬(Ibuprofen,4-25)为苯丙酸类环氧合酶COX抑制剂,具有解热、镇痛、抗炎等作用,解热疗效突出,安全性好,是临床上最为常用的非甾体抗炎药。目前,文献报道的布洛芬的合成路线多达20余条,各有优缺点,以下列举并分析几种具有代表性的路线。
路线(1)如图4-9,以乙苯为原料(4-26),与异丁酰氯发生酰化反应得4-异丁基乙苯(4-27),4-异丁基乙苯(4-27)在溴化剂溴代- N -丁二酰亚胺(NBS)作用下制得相应的溴代物(4-28),溴代物与氰化钠反应引入氰基,氰化物(4-29)在碱性条件下水解成酸(4-30),最后经还原反应制得布洛芬(4-25)。此法中,氰化反应用到剧毒氰化钠,酰化反应中酰氯的刺激性也较大,NBS价格也略贵,整体原料成本大,工业化价值不大。
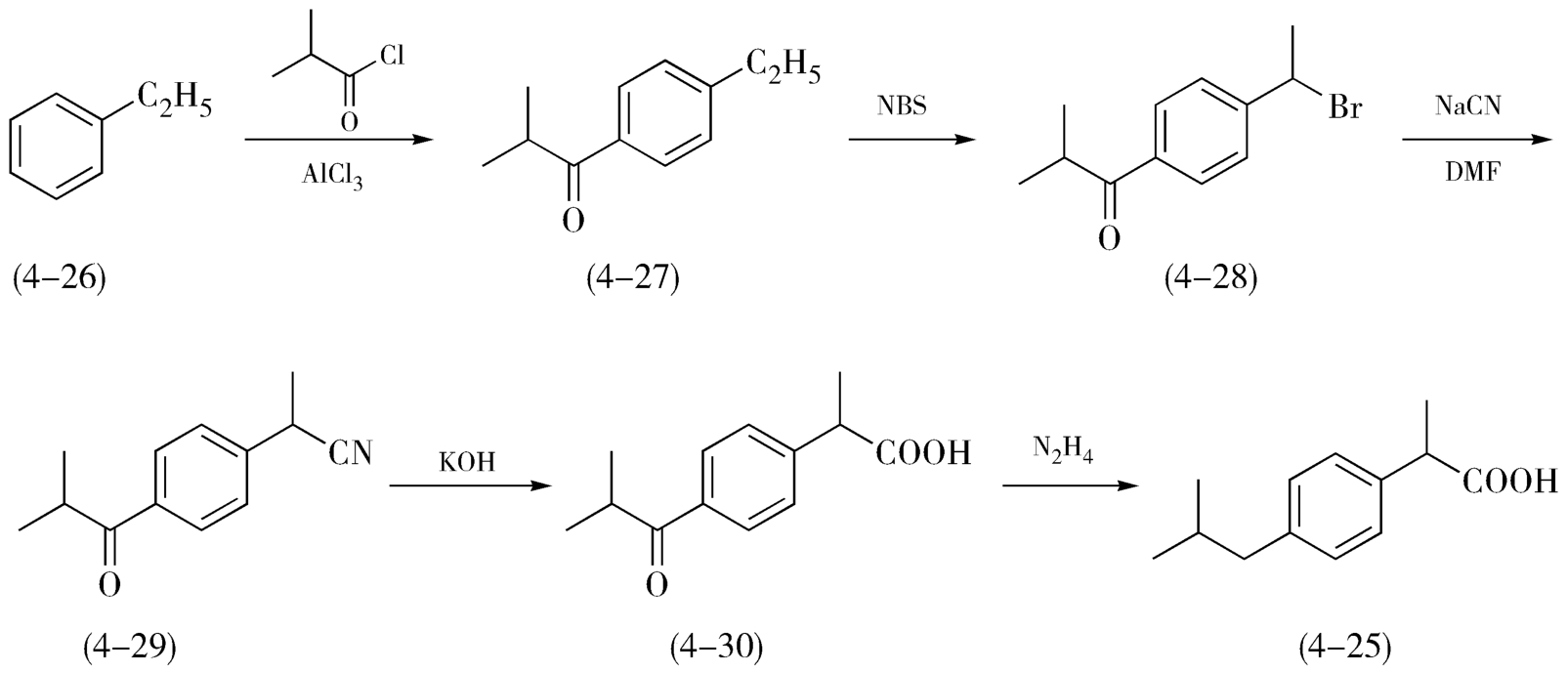
图4-9 以乙苯为起始原料合成布洛芬的路线图
路线(2)如图4-10,以异丁基苯乙酮(4-31)为原料,与氯仿在相转移催化剂的存在下发生反应,得到中间体酸(4-32),中间体酸(4-32)再经氢化还原制得布洛芬(4-25)。反应条件要求较高,两步反应的选择性都不高,副反应较多。
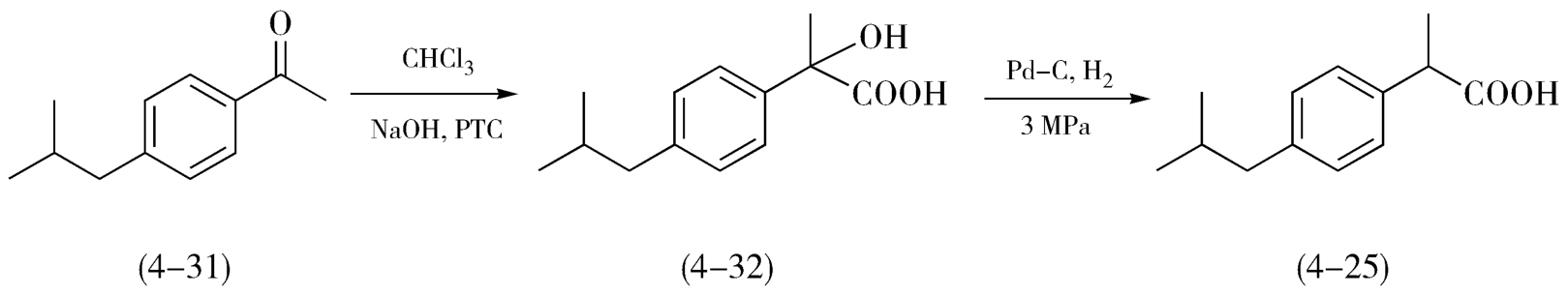
图4-10 以异丁基苯乙酮为起始原料合成布洛芬的路线图
路线(3)如图4-11,以异丁基氯代乙苯(4-34)为原料,经格式反应制得布洛芬(4-25)。整体收率较高,但需用到格式试剂,格氏反应为严格无水、无氧反应,条件苛刻,且格式试剂须自制,原料价格昂贵,乙醚易燃易爆,因此,此路线不适于工业化生产。
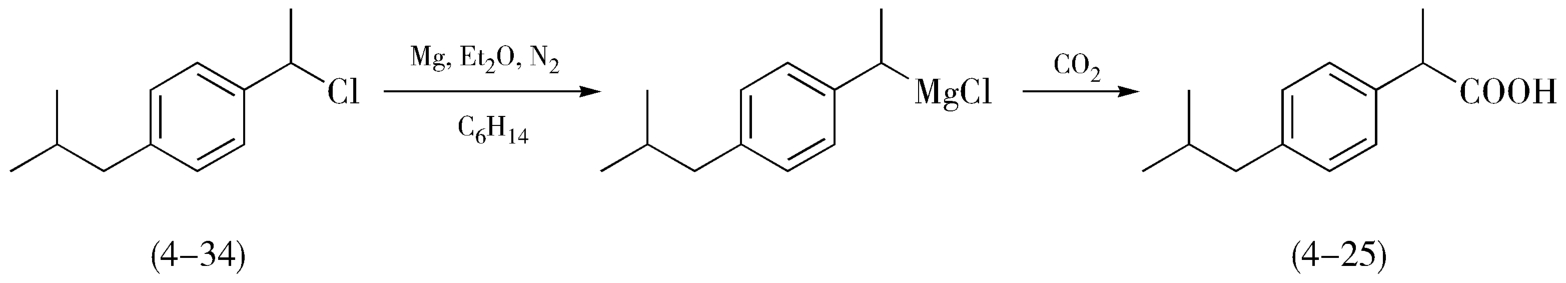
图4-11 以异丁基苯乙酮为起始原料合成布洛芬的路线图
路线(4)如图4-12,是以异丁基苯(4-35)为起始原料,异丁基苯与对甲苯磺酸酯(4-36)在过量的AlCl 3 存在下,一步反应生成布洛芬。该路线短且简捷,主要缺点是产生大量异构体,产品质量差,收率低。
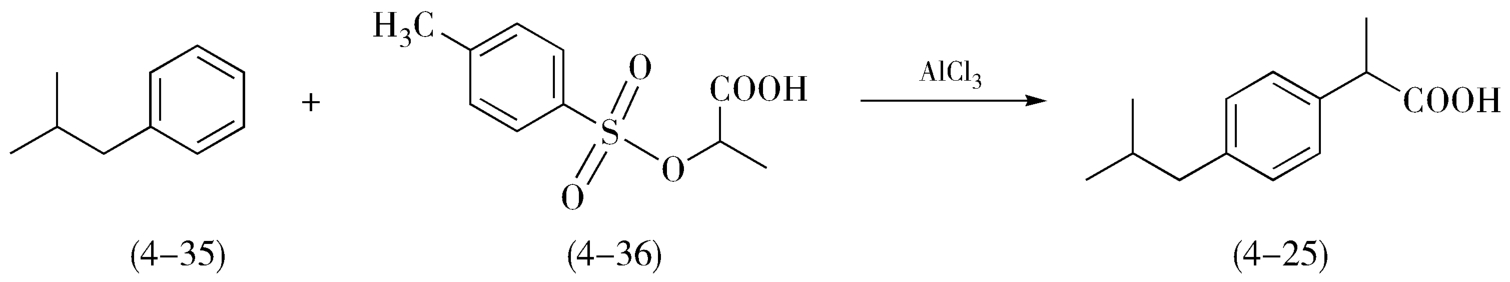
图4-12 异丁基苯与乳酸衍生物一步法合成布洛芬的路线图
路线(5)如图4-13,以异丁基苯为原料,以甲醛为甲基化试剂,制得相应卤代烷(4-37),此氯化物和氰化钠反应得中间体异丁基苯乙腈(4-38),此腈化物(4-38)再经甲基化、氰基水解,制得布洛芬。此路线中由于用到剧毒氰化物,故操作要求高,且存在设备腐蚀和“三废”处理问题。
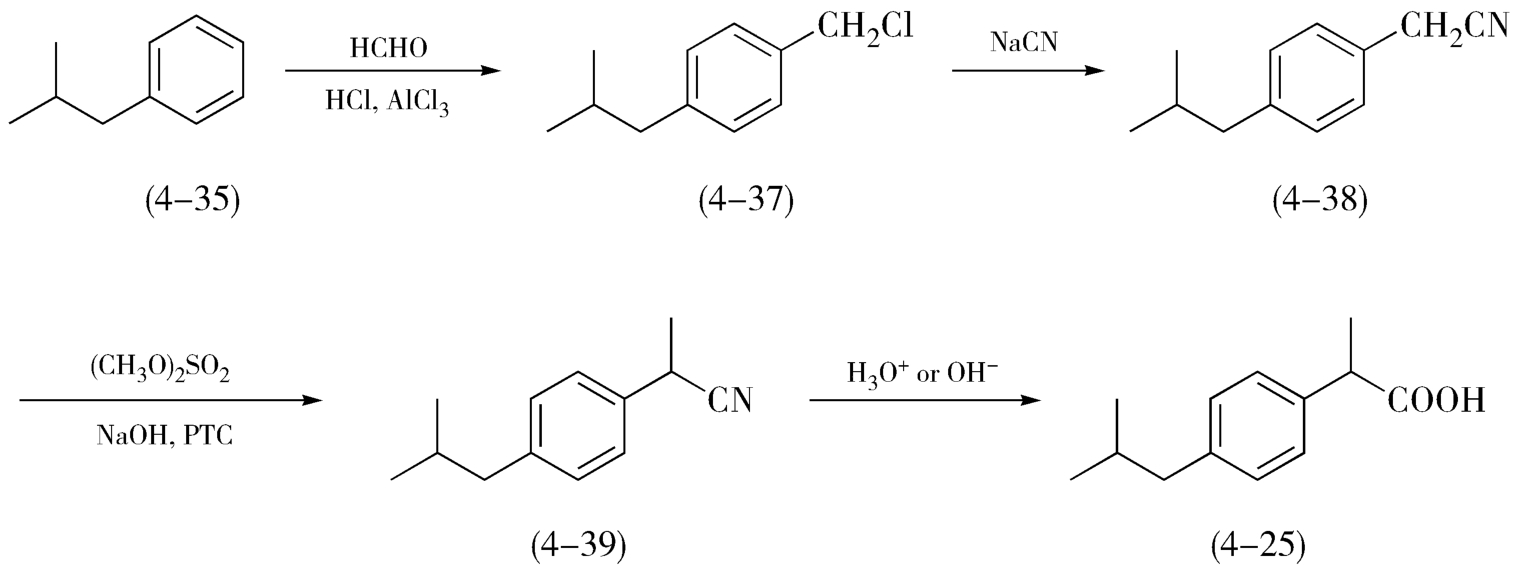
图4-13 氰化物法合成布洛芬的路线图
环氧羧酸酯法是Boots公司开发的以异丁苯为原料的成熟的工艺路线,曾被国内外多家药厂所采用,也称Boots法,如图4-14所示。原料异丁苯(4-35)在三氯化铝的催化下与醋酸酐发生Friedel-Crafts酰基化反应得到对异丁基苯乙酮(4-31),后者在乙醇钠的作用下与氯乙酸乙酯发生Darzen缩合反应,制得的环氧丁酸酯类化合物(4-40),再经过水解脱羧反应得到异丁基苯丙醛(4-41)。异丁基苯丙醛(4-41)可经重铬酸钠氧化得布洛芬,也可经成肟、水解得到布洛芬(4-25)。该路线原料易得、反应可靠、控制方便,是较为成熟的工业化路线。但是随着技术的不断发展,对生产效率的要求越来越高,此路线还存在优化的空间,其不足之处有路线较长、反应过程中需要使用醇钠、存在一定的安全隐患、原子利用率较低、成品的精制过程较复杂、生产成本相对较高。
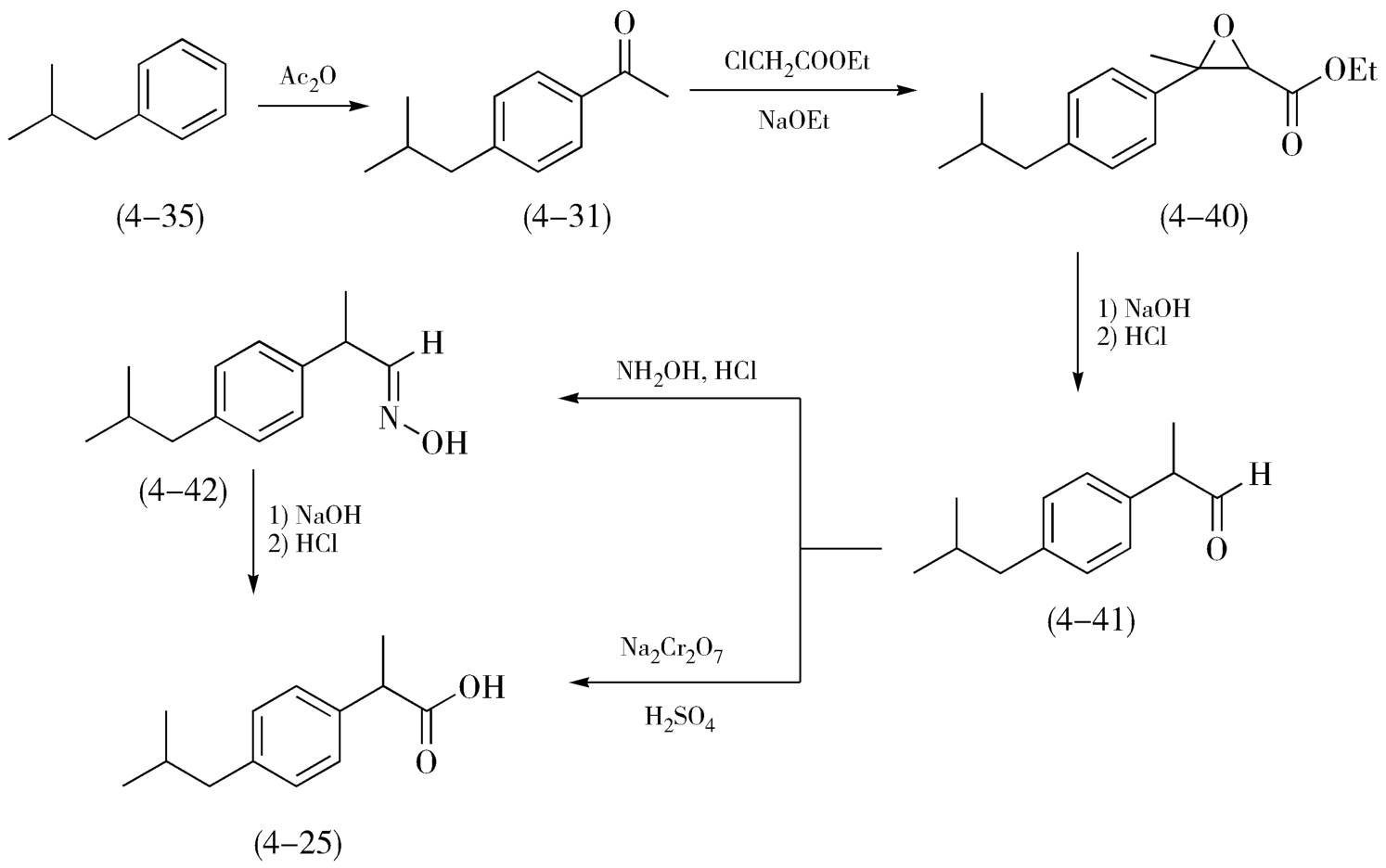
图4-14 Boots法合成布洛芬的路线图
1992年美国Hoechst-Celanese公司与Boots公司联合开发了一条全新的3步法合成布洛芬的工艺路线,即“BHC”路线。该路线仍以异丁苯(4-35)为起始原料,在HF的催化下与醋酸酐发生Friedel-Crafts酰基化反应得到对异丁基苯乙酮(4-31),在Raney Ni的催化下,异丁基苯乙酮(4-31)发生氢化还原反应,得到对异丁基苯乙醇(4-43),在金属有机络合催化剂Pd(Ⅱ)的催化下,苯乙醇衍生物在高压(>16Mpa)下与CO发生插羰反应,生成布洛芬(4-25)(图4-15)。与经典的6步法路线相比,3步法路线的优点十分突出:①反应步骤减少,路线明显缩短。②原料和试剂的种类减少,价格低廉,无需使用溶剂。③气态催化剂HF方便循环使用;金属Ni催化后处理容易;贵金属有机催化剂PdCl 2 (PPh 3 ) 2 催化效率高、选择性好。④后处理次数减少,产物的纯度良好。⑤3步反应收率都很高,总收率可达92.2%。⑥尤为重要的是,该路线的原子经济性非常高。
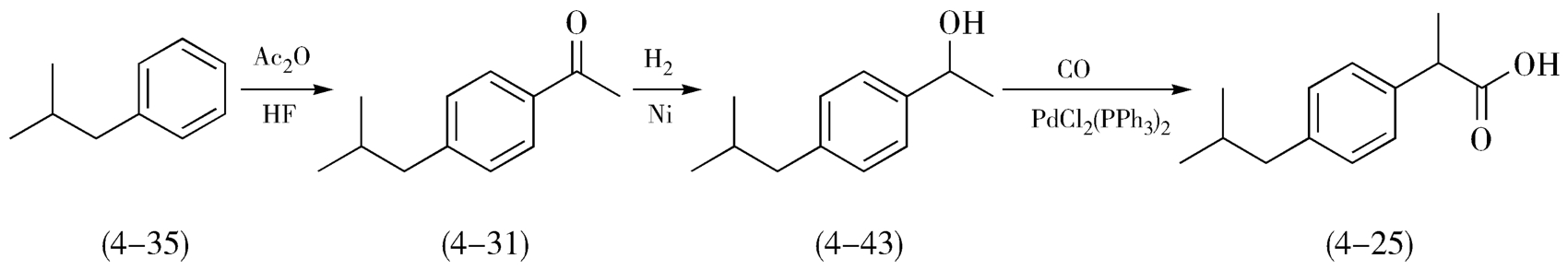
图4-15 BHC法合成布洛芬的路线图
一般情况下,关于一个药物的合成路线可能有很多条,他们的合成途径各有特点,我们把有利于工业化生产的路线称为工艺路线,在诸多的合成路线中选择最有工业生产价值的路线。由以上典型药物工艺路线的评价可以看出,工艺路线的选择需考虑到路线、原料、反应条件、纯化方法、设备、绿色环保等方方面面的问题,必须通过综合比较和深入的实践验证。