




机体运动过程中会消耗大量的ATP以提供能量,再通过对碳水化合物(肌糖原和血糖)和脂肪酸(肌内脂肪和血脂)的氧化补充ATP的损耗。在运动的起始阶段,血糖对ATP再合成的作用并不很大。但是,随着运动时间的延长,肌糖原大量消耗,血糖渐变成一种重要的代谢底物,最多可达到总氧化供能比例的35%(而几乎100%的碳水化合物氧化底物为血糖)。运动过程中肌肉摄取的葡萄糖主要用于糖酵解和随后的氧化。有规律的运动锻炼能提高机体的糖耐量水平,研究显示,Ⅱ型糖尿病人在一次急性运动后其血糖水平就有明显下降,
 说明即使机体胰岛素功能不全,运动也可以刺激骨骼肌葡萄糖的吸收增加。因此,运动诱导骨骼肌对葡萄糖摄取被认为是通过有别于胰岛素的作用途径而实现的。
说明即使机体胰岛素功能不全,运动也可以刺激骨骼肌葡萄糖的吸收增加。因此,运动诱导骨骼肌对葡萄糖摄取被认为是通过有别于胰岛素的作用途径而实现的。
机体内有三个位点调节骨骼肌的葡萄糖摄取:血液运输葡萄糖的能力;肌细胞膜对葡萄糖的转运能力;肌细胞内葡萄糖的磷酸化。
 它们是单独还是协同调节骨骼肌对葡萄糖的利用很难区分,我们加以分述。
它们是单独还是协同调节骨骼肌对葡萄糖的利用很难区分,我们加以分述。
组织葡萄糖的供应取决于血流量和血糖浓度两方面。在剧烈运动时,肌肉的血流量可以增加近20 倍,并且可能在肌内会重新分布
 ,肌肉血流量的增加对于骨骼肌葡萄糖供应提供了在数量上的重要保证。在体外进行的对大鼠前肢电刺激的灌流实验显示血流量对于收缩肌的葡萄糖摄取有重要影响。
,肌肉血流量的增加对于骨骼肌葡萄糖供应提供了在数量上的重要保证。在体外进行的对大鼠前肢电刺激的灌流实验显示血流量对于收缩肌的葡萄糖摄取有重要影响。
 但是是否血液流量限制正常的骨骼肌收缩中葡萄糖摄取却有待研究。因为,如果血流量是运动时骨骼肌摄取葡萄糖的限制因素,那么在运动的间隙时间,血糖浓度应该会有所下降。但是,事实是运动间隙时间血糖浓度依然高于安静状态。
但是是否血液流量限制正常的骨骼肌收缩中葡萄糖摄取却有待研究。因为,如果血流量是运动时骨骼肌摄取葡萄糖的限制因素,那么在运动的间隙时间,血糖浓度应该会有所下降。但是,事实是运动间隙时间血糖浓度依然高于安静状态。
另一方面,在离体肌肉收缩实验
 和在体实验
和在体实验
 研究中发现:在胰岛素水平不上升的前提下,可以通过增加血糖浓度从而增加肌肉的葡萄糖供应,并因此提高肌肉的葡萄糖摄取。相反,在长时间的运动导致血糖浓度下降时,腿部肌肉对葡萄糖的摄取也下降。在正常的生理范围内,血糖浓度和骨骼肌的葡萄糖摄取几乎是一种线形关系。这就提示:运动中肌肉的葡萄糖摄取多少和血糖浓度的变化是密切相关的。
研究中发现:在胰岛素水平不上升的前提下,可以通过增加血糖浓度从而增加肌肉的葡萄糖供应,并因此提高肌肉的葡萄糖摄取。相反,在长时间的运动导致血糖浓度下降时,腿部肌肉对葡萄糖的摄取也下降。在正常的生理范围内,血糖浓度和骨骼肌的葡萄糖摄取几乎是一种线形关系。这就提示:运动中肌肉的葡萄糖摄取多少和血糖浓度的变化是密切相关的。
综上所述,运动过程中肌肉血流量的增加可能是对骨骼肌代谢要求的一种适应,在健康机体并不是骨骼肌摄取葡萄糖的限制因素;血糖浓度才是运动时骨骼肌摄取葡萄糖的主要限制因素。
骨骼肌表达多种葡萄糖转运体(glucose transporters,GLUT)的异构体,其中对运动过程中骨骼肌摄取葡萄糖影响最大的是GLUT4。

体外实验证实,全身
 或骨骼肌特异性
或骨骼肌特异性
 GLUT4缺失时,运动就不再引起骨骼肌摄取葡萄糖的增加。有些研究显示GLUT4 是运动时骨骼肌摄取葡萄糖的限制因素。Derave等
GLUT4缺失时,运动就不再引起骨骼肌摄取葡萄糖的增加。有些研究显示GLUT4 是运动时骨骼肌摄取葡萄糖的限制因素。Derave等
 利用大鼠进行的实验已证实,骨骼肌膜的GLUT4 含量和运动中骨骼肌摄取葡萄糖的多少密切相关。人体实验
利用大鼠进行的实验已证实,骨骼肌膜的GLUT4 含量和运动中骨骼肌摄取葡萄糖的多少密切相关。人体实验
 也表明在中等强度的运动时,葡萄糖的转运速率是骨骼肌摄取葡萄糖的限制因素。但是,在高强度运动时肝糖原分解非常快,6-磷酸葡萄糖(glucose -6 - phosphate,G6P)生成较多,抑制了己糖激酶(hexokinase,HK)活性,从而使得葡萄糖的磷酸化速度成为主要的限制因素。
也表明在中等强度的运动时,葡萄糖的转运速率是骨骼肌摄取葡萄糖的限制因素。但是,在高强度运动时肝糖原分解非常快,6-磷酸葡萄糖(glucose -6 - phosphate,G6P)生成较多,抑制了己糖激酶(hexokinase,HK)活性,从而使得葡萄糖的磷酸化速度成为主要的限制因素。
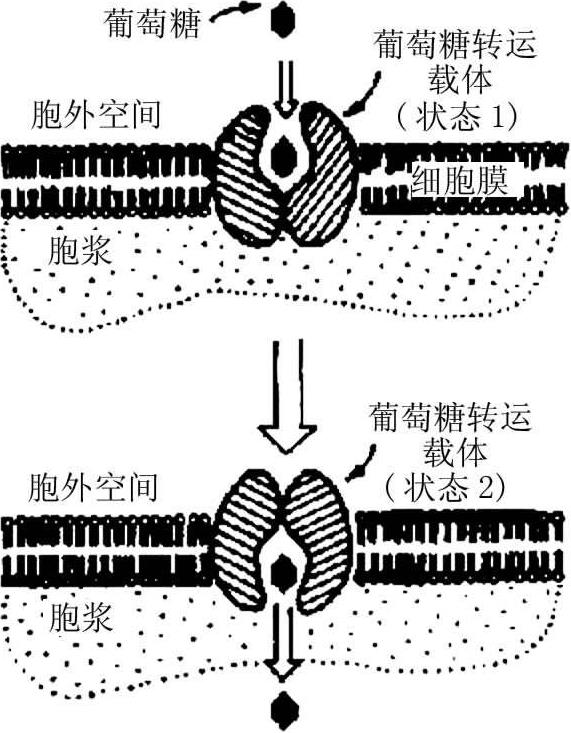
图1 -3 肌细胞膜对葡萄糖的转运
研究显示,
 运动只会影响葡萄糖转运的Vmax而不改变GLUT4的Km,这表明运动会诱导肌细胞膜的GLUT4数目增加,但对其亲和力影响不大。已经证实,运动和胰岛素一样可以增加肌细胞表面和横管的GLUT4数目。Wasserman和colleagues的研究
运动只会影响葡萄糖转运的Vmax而不改变GLUT4的Km,这表明运动会诱导肌细胞膜的GLUT4数目增加,但对其亲和力影响不大。已经证实,运动和胰岛素一样可以增加肌细胞表面和横管的GLUT4数目。Wasserman和colleagues的研究

 证实,GLUT4 的过分表达或部分缺失并不改变在体骨骼肌运动中对血液葡萄糖摄取。这说明在正常情况下运动过程中肌膜表面的GLUT4 数目增加只是对骨骼肌摄取葡萄糖起到允许的作用,而非限制因素;或者运动诱导肌膜表面的GLUT4增加仅仅是动用了肌细胞内“GLUT4总池”中的一部分。
证实,GLUT4 的过分表达或部分缺失并不改变在体骨骼肌运动中对血液葡萄糖摄取。这说明在正常情况下运动过程中肌膜表面的GLUT4 数目增加只是对骨骼肌摄取葡萄糖起到允许的作用,而非限制因素;或者运动诱导肌膜表面的GLUT4增加仅仅是动用了肌细胞内“GLUT4总池”中的一部分。
引起骨骼肌GLUT4转位的分子机制非常复杂。
 现在已经很清楚骨骼肌内分别存在对胰岛素和运动做出反应的不同的“GUT4 池”。
现在已经很清楚骨骼肌内分别存在对胰岛素和运动做出反应的不同的“GUT4 池”。
 胰岛素和运动诱导GLUT4转位并增加骨骼肌葡萄糖摄取的分子信号是不同的
[1]
:胰岛素引起rab4蛋白分布的变化,而运动引起转铁蛋白受体的重新分布。尽管这样,二者之间还是有相似性,运动和胰岛素都能引起胰岛素应答氨基肽酶
胰岛素和运动诱导GLUT4转位并增加骨骼肌葡萄糖摄取的分子信号是不同的
[1]
:胰岛素引起rab4蛋白分布的变化,而运动引起转铁蛋白受体的重新分布。尽管这样,二者之间还是有相似性,运动和胰岛素都能引起胰岛素应答氨基肽酶
 和肌膜上GTP接合蛋白的浓度变化。肌膜表面的GLUT4含量增加到底是因为细胞内吞作用的减少还是外分泌增加所致并不清楚,但是目前的研究比较支持后者。
和肌膜上GTP接合蛋白的浓度变化。肌膜表面的GLUT4含量增加到底是因为细胞内吞作用的减少还是外分泌增加所致并不清楚,但是目前的研究比较支持后者。

Fueger等还利用骨骼肌中HKⅡ过分表达或部分缺失的大鼠在体实验证实,HK Ⅱ在运动诱导的骨骼肌葡萄糖摄取增加中有重要作用。


 但是,骨骼肌HKⅡ部分缺失大鼠运动中对骨骼肌摄取葡萄糖的限制只体现在氧化型骨骼肌纤维,而对混和型骨骼肌纤维则没有明显的影响。考虑到人体骨骼肌纤维类型的不同,这一结果推至人体还尚待进一步的研究。在HKⅡ活性较低的Ⅱ型糖尿病人,骨骼肌对葡萄糖的摄取还可以保持正常,可能是因为葡萄糖的运送和GLUT4 的活性并没有受到伤害。还有少数的研究
但是,骨骼肌HKⅡ部分缺失大鼠运动中对骨骼肌摄取葡萄糖的限制只体现在氧化型骨骼肌纤维,而对混和型骨骼肌纤维则没有明显的影响。考虑到人体骨骼肌纤维类型的不同,这一结果推至人体还尚待进一步的研究。在HKⅡ活性较低的Ⅱ型糖尿病人,骨骼肌对葡萄糖的摄取还可以保持正常,可能是因为葡萄糖的运送和GLUT4 的活性并没有受到伤害。还有少数的研究
 表明,在急性的运动或长时间练习后哺乳动物的HKⅡ活性会发生改变,但是没有研究证实急性运动引起的HKⅡ活性变化和运动导致葡萄糖摄取增加间有何联系。
表明,在急性的运动或长时间练习后哺乳动物的HKⅡ活性会发生改变,但是没有研究证实急性运动引起的HKⅡ活性变化和运动导致葡萄糖摄取增加间有何联系。
但是,HKⅡ活性的明显降低很有可能是一些情况下骨骼肌摄取葡萄糖的限制因素。根据目前的研究,较为统一的观点包括
 :1.葡萄糖磷酸化是骨骼肌摄取葡萄糖的一个重要步骤,受到HK异构体的调节。2.基础状态时,葡萄糖转运可能是机体摄取葡萄糖的主要限制因素,但是在运动和胰岛素功能亢进时,葡萄糖磷酸化则是一个重要的限速步骤。3.高脂肪饮食损害机体胰岛素和/或运动引起的骨骼肌摄取葡萄糖,主要是影响HK活力,从而影响葡萄糖的磷酸化。总体说,HK活性对运动中骨骼肌葡萄糖摄取的调节还是很不明确,也有可能仅仅在高强度运动导致G6P大量积累而抑制HK活性的时候才体现出来,因此,运动也被认为是诊断机体是否葡萄糖磷酸化功能不全的重要手段。
:1.葡萄糖磷酸化是骨骼肌摄取葡萄糖的一个重要步骤,受到HK异构体的调节。2.基础状态时,葡萄糖转运可能是机体摄取葡萄糖的主要限制因素,但是在运动和胰岛素功能亢进时,葡萄糖磷酸化则是一个重要的限速步骤。3.高脂肪饮食损害机体胰岛素和/或运动引起的骨骼肌摄取葡萄糖,主要是影响HK活力,从而影响葡萄糖的磷酸化。总体说,HK活性对运动中骨骼肌葡萄糖摄取的调节还是很不明确,也有可能仅仅在高强度运动导致G6P大量积累而抑制HK活性的时候才体现出来,因此,运动也被认为是诊断机体是否葡萄糖磷酸化功能不全的重要手段。

总而言之,葡萄糖的供应、转运和磷酸化是运动过程中骨骼肌摄取葡萄糖的重要调节步骤。是否一个或几个因素一起调节机体的葡萄糖摄取还很难区分,因为所有的因素都和骨骼肌的能量状况以及骨骼肌纤维的募集紧密相关。也有可能是氧化型肌纤维更多地依赖于葡萄糖的供应和HK的活性,而酵解型肌纤维则更多地取决于葡萄糖的转运。还可以假定,即使在同一骨骼肌纤维内,其摄取葡萄糖的限制因素也会因为运动强度、运动时间、肌糖原状况和血糖浓度不同而变化。
胰岛素刺激骨骼肌对葡萄糖转运增加的信号机制还不是十分明了,而运动引起的葡萄糖转运增加和刺激GLUT4转位的机制则更知之甚少。一般认为其信号应该不依赖于激素而是更多地由于收缩肌肉本身分泌的一些旁分泌因子在起作用。事实上有很多的研究证明离体的骨骼肌收缩也会引起葡萄糖转运的增加。笔者认为,对一些肌肉模型(比如离体灌流的后肢或实验室培养的肌细胞)进行研究可能会得到更为深刻的结果。因为在这样的条件下,肌肉的葡萄糖供应可以得到严格的控制。
几乎30年前,肌肉收缩引起的瞬时性的肌内Ca
2
+
浓度上升就被假定为与肌肉收缩诱导的葡萄糖转运增加有关。
 因为肌内Ca
2+
浓度上升与运动神经元的冲动相关,所以Ca
2+
浓度变化引起的相关信号调节被认为是一种前馈调节。利用蛙的缝匠肌和咖啡因培育,可以引起肌浆网释放Ca
2+
。研究发现
[2]
,将大鼠的股四头肌和咖啡因一起孵育也可以提高肌细胞内的Ca
2+
浓度,同时增加肌细胞的葡萄糖摄取。但是,其他的一些离体实验却没有发现相类似的结果。
[3]
这些研究的差异很不好解释,可能是由于引起Ca
2
+
释放的数量和其在胞浆中持续作用的时间长短不同所引起。
因为肌内Ca
2+
浓度上升与运动神经元的冲动相关,所以Ca
2+
浓度变化引起的相关信号调节被认为是一种前馈调节。利用蛙的缝匠肌和咖啡因培育,可以引起肌浆网释放Ca
2+
。研究发现
[2]
,将大鼠的股四头肌和咖啡因一起孵育也可以提高肌细胞内的Ca
2+
浓度,同时增加肌细胞的葡萄糖摄取。但是,其他的一些离体实验却没有发现相类似的结果。
[3]
这些研究的差异很不好解释,可能是由于引起Ca
2
+
释放的数量和其在胞浆中持续作用的时间长短不同所引起。
一些研究力图通过对Ca
2+
激活的一些酶的活性变化检测来确定Ca
2+
的作用。蛋白激酶C (protein kinase C,PKC)可以被肌内Ca
2+
和甘油二脂(diacylglycerol,DAG)浓度的升高而激活。大鼠运动或肌肉收缩时,骨骼肌的PKC活性会升高
 ,但是在人体没有观察到这种现象。
,但是在人体没有观察到这种现象。
 另外,PKC活性的缓慢下调或化学抑制可以减少运动诱导的骨骼肌葡萄糖转运增加。虽然有些研究显示PKC可能与收缩引起骨骼肌摄取葡萄糖增加有关,但是对于其参与这一过程的确切机制还需要更深入的研究。
另外,PKC活性的缓慢下调或化学抑制可以减少运动诱导的骨骼肌葡萄糖转运增加。虽然有些研究显示PKC可能与收缩引起骨骼肌摄取葡萄糖增加有关,但是对于其参与这一过程的确切机制还需要更深入的研究。
另一种无处不在的Ca
2+
敏感的蛋白是CaM (calmodulin)。研究显示,抑制CaM活性会减少运动诱导的骨骼肌葡萄糖摄取。但是,这种作用也可能是由于CaM降低骨骼肌紧张性所致,因为CaM参与骨骼肌内很多信号途径(包括兴奋-收缩藕连)。
 然而,利用KN62 /93 特异性阻断Ca
2+
接合CaM后激活的一些多功能蛋白激酶(Ca
2+
- bound CaM kinase,CaMK),会抑制大鼠离体比目鱼肌的葡萄糖摄取。
[4]
人体和啮齿动物运动时,其收缩肌内CaMKⅡ活性会升高,而KN62 /93可以抑制机体由于运动引起的CaMKⅡ活性升高。虽然CaMKⅡ是KN62 /93的一种靶分子,但是CaMKI也不能完全排除在外。事实上CaMKI也是在骨骼肌内表达,而CaMKⅣ却不在骨骼肌内表达。胰岛素刺激骨骼肌摄取葡萄糖的作用也可以被KN62部分抑制,这说明胰岛素的活性可能也部分地依赖于CaMK,但是也可能是由于KN62对葡萄糖转运的抑制没有特异性所致。
然而,利用KN62 /93 特异性阻断Ca
2+
接合CaM后激活的一些多功能蛋白激酶(Ca
2+
- bound CaM kinase,CaMK),会抑制大鼠离体比目鱼肌的葡萄糖摄取。
[4]
人体和啮齿动物运动时,其收缩肌内CaMKⅡ活性会升高,而KN62 /93可以抑制机体由于运动引起的CaMKⅡ活性升高。虽然CaMKⅡ是KN62 /93的一种靶分子,但是CaMKI也不能完全排除在外。事实上CaMKI也是在骨骼肌内表达,而CaMKⅣ却不在骨骼肌内表达。胰岛素刺激骨骼肌摄取葡萄糖的作用也可以被KN62部分抑制,这说明胰岛素的活性可能也部分地依赖于CaMK,但是也可能是由于KN62对葡萄糖转运的抑制没有特异性所致。
一氧化氮合成酶(Nitric oxide synthase,NOS)可以被Ca
2
+
接合的CaM所激活。
 已有一些研究显示啮齿动物在运动过程中NOS活性会上升,NO生成增多。一些研究显示骨骼肌被施以NOS抑制剂后减少了其运动所致葡萄糖摄取增加,
已有一些研究显示啮齿动物在运动过程中NOS活性会上升,NO生成增多。一些研究显示骨骼肌被施以NOS抑制剂后减少了其运动所致葡萄糖摄取增加,
 而有些研究则认为没有影响。
而有些研究则认为没有影响。

 对人体运动肢进行的在体实验显示NOS活性抑制减少骨骼肌的葡萄糖摄取,而不影响其总的血流量。
对人体运动肢进行的在体实验显示NOS活性抑制减少骨骼肌的葡萄糖摄取,而不影响其总的血流量。
 但是这没有排除NOS被抑制后对葡萄糖供应的影响,因为这些抑制因素可能会影响内皮细胞的NOS活性,而NO有利于在运动中增加微循环以提供营养。因为在总血流量不变的前提下,运动肌肉赖以得到营养的微循环是可以变化的。
但是这没有排除NOS被抑制后对葡萄糖供应的影响,因为这些抑制因素可能会影响内皮细胞的NOS活性,而NO有利于在运动中增加微循环以提供营养。因为在总血流量不变的前提下,运动肌肉赖以得到营养的微循环是可以变化的。
 抑制NOS活性对运动中骨骼肌葡萄糖摄取的影响可能是由于其对葡萄糖供应的影响,而不是在于其对葡萄糖的转运,但是这还需要进一步的研究加以证实。
抑制NOS活性对运动中骨骼肌葡萄糖摄取的影响可能是由于其对葡萄糖供应的影响,而不是在于其对葡萄糖的转运,但是这还需要进一步的研究加以证实。
已有研究
 观察到肌内的磷酸肌酸浓度和肌肉收缩诱导的葡萄糖摄取间有种负相关性,这提示在肌肉的能量状况和其葡萄糖摄取间有一种信号传递。这可以认为是肌肉葡萄糖摄取的一种反馈调节机制。近来的研究显示,AMP激活蛋白激酶(5- AMP - activated protein kinase,AMPK)可能就是这样一种信号分子。
观察到肌内的磷酸肌酸浓度和肌肉收缩诱导的葡萄糖摄取间有种负相关性,这提示在肌肉的能量状况和其葡萄糖摄取间有一种信号传递。这可以认为是肌肉葡萄糖摄取的一种反馈调节机制。近来的研究显示,AMP激活蛋白激酶(5- AMP - activated protein kinase,AMPK)可能就是这样一种信号分子。
 AMPK是一种多功能的丝氨酸/苏氨酸蛋白激酶,它灵敏地受到肌内的AMP/ ATP和C / CP比率变化的调节,从而反应运动肌肉的能量状况。运动和肌肉收缩可以提高肌内的AMPK活性
AMPK是一种多功能的丝氨酸/苏氨酸蛋白激酶,它灵敏地受到肌内的AMP/ ATP和C / CP比率变化的调节,从而反应运动肌肉的能量状况。运动和肌肉收缩可以提高肌内的AMPK活性


 ,AMPK激活数量具有运动强度依赖性。在安静肉,AICAR (5 - aminoimidazole -4 - carboxyamide - ribonucleoside)可以激活AMPK,进而增加肌肉对葡萄糖的转运和摄取
,AMPK激活数量具有运动强度依赖性。在安静肉,AICAR (5 - aminoimidazole -4 - carboxyamide - ribonucleoside)可以激活AMPK,进而增加肌肉对葡萄糖的转运和摄取
 ,因此似乎从逻辑上可以认为AMPK在收缩引起的骨骼肌葡萄糖摄取增加中有重要意义。
,因此似乎从逻辑上可以认为AMPK在收缩引起的骨骼肌葡萄糖摄取增加中有重要意义。
但是,利用基因技术对AMPK的接合亚基
 或调节亚基
或调节亚基
 敲除,以及增加非活性AMPK表达
敲除,以及增加非活性AMPK表达
 PK是否与收缩引起的骨骼肌葡萄糖摄取增加有关这一问题上得到一些矛盾的结果。虽然基因敲除后,AICAR增加骨骼肌葡萄糖摄取的功能消失
PK是否与收缩引起的骨骼肌葡萄糖摄取增加有关这一问题上得到一些矛盾的结果。虽然基因敲除后,AICAR增加骨骼肌葡萄糖摄取的功能消失

 ,但是AMPK的活性变化仅仅受到部分的影响。
,但是AMPK的活性变化仅仅受到部分的影响。


 Mu
Mu
 的研究显示,在AMPK酶活性完全受到抑制的骨骼肌内,运动导致的葡萄糖摄取增加仅仅下降30 ~ 40%。另外,利用灌流的大鼠前肢肌肉的研究显示,AMPK和骨骼肌葡萄糖摄取的相关性主要体现在快肌纤维,而在慢肌纤维则没有相关性,因此AMPK可能在不同类型的肌纤维中起不同作用。
的研究显示,在AMPK酶活性完全受到抑制的骨骼肌内,运动导致的葡萄糖摄取增加仅仅下降30 ~ 40%。另外,利用灌流的大鼠前肢肌肉的研究显示,AMPK和骨骼肌葡萄糖摄取的相关性主要体现在快肌纤维,而在慢肌纤维则没有相关性,因此AMPK可能在不同类型的肌纤维中起不同作用。
 人体实验
人体实验
 也证实了在快肌纤维中,AMPK活性和肌肉的葡萄糖摄取有相互的关联。
也证实了在快肌纤维中,AMPK活性和肌肉的葡萄糖摄取有相互的关联。
因此,虽然AMPK是一种调节肌肉收缩所致葡萄糖摄取的很有吸引力的信号,但是因为目前的不同研究结果和争议,所以其确切的作用还有待于进一步的研究证实。至少,在AMPK活性和肌肉收缩过程中葡萄糖摄取间不会是一个简单的剂量依存关系。
因为运动和胰岛素都可以刺激骨骼肌摄取葡萄糖增加,很自然地就会提到在这二者之间是否有一些共同的蛋白质在起作用。已经证实运动不会增加胰岛素受体(insulin receptor,IR)和胰岛素受体底物(insulin receptorsubstrate,IR - S )的酪氨酸磷酸化水平。
 同时,研究
同时,研究

 发现运动也不会提高骨骼肌的磷脂酰肌醇-3 -激酶(phosphatidylinositol 3 - kinase,PI3K)的水平,抑制PI3K的活性
发现运动也不会提高骨骼肌的磷脂酰肌醇-3 -激酶(phosphatidylinositol 3 - kinase,PI3K)的水平,抑制PI3K的活性
 也不影响收缩所致骨骼肌葡萄糖摄取的增加。但是,PI3K的抑制剂渥曼青霉素可以减少灌流的前肢肌肉的葡萄糖摄取。
也不影响收缩所致骨骼肌葡萄糖摄取的增加。但是,PI3K的抑制剂渥曼青霉素可以减少灌流的前肢肌肉的葡萄糖摄取。
 这些在体的
这些在体的
 和灌流的
和灌流的
 实验所以有不同的结果可能是因为灌流液中缺少某些在体实验中具有的刺激因子(比如神经因子)所致。
实验所以有不同的结果可能是因为灌流液中缺少某些在体实验中具有的刺激因子(比如神经因子)所致。
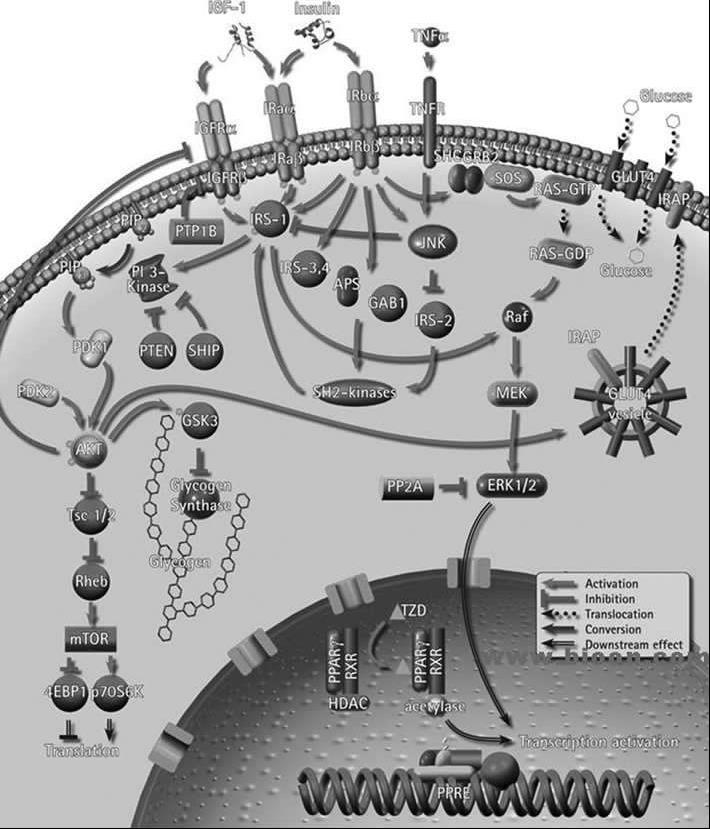
图1 -4 胰岛素信号通路图
一些

 但并非所有
但并非所有
 的研究表明,运动会提高蛋白激酶B(protein kinase B,PKB)的活力和磷酸化过程。PKB的AS160 亚基磷酸化与GLUT4转位及胰岛素刺激的脂肪细胞葡萄糖转运有关
的研究表明,运动会提高蛋白激酶B(protein kinase B,PKB)的活力和磷酸化过程。PKB的AS160 亚基磷酸化与GLUT4转位及胰岛素刺激的脂肪细胞葡萄糖转运有关
 ,而运动也可以刺激啮齿动物骨骼肌的AS160 亚基磷酸化。
,而运动也可以刺激啮齿动物骨骼肌的AS160 亚基磷酸化。
 但是,也有研究显示,PKB敲除并不影响大鼠比目鱼肌的运动诱导的骨骼肌葡萄糖摄取增加。
但是,也有研究显示,PKB敲除并不影响大鼠比目鱼肌的运动诱导的骨骼肌葡萄糖摄取增加。
还有研究显示



 运动会提高运动肌中非特异性蛋白激酶C (Atypical protein kinase C,aPKC)的活性,但是其机制并不清楚。因为aPKC也是胰岛素引起肌肉葡萄糖摄取增加的一种信号,所以aPKC也可能是运动引起骨骼肌葡萄糖摄取的一种信号,但是目前还没有直接证据能证明这一假说。
运动会提高运动肌中非特异性蛋白激酶C (Atypical protein kinase C,aPKC)的活性,但是其机制并不清楚。因为aPKC也是胰岛素引起肌肉葡萄糖摄取增加的一种信号,所以aPKC也可能是运动引起骨骼肌葡萄糖摄取的一种信号,但是目前还没有直接证据能证明这一假说。
总之,运动过程中骨骼肌对葡萄糖的摄取增加可能由于血液葡萄糖供应增多,肌膜表面的葡萄糖转运加快及细胞内葡萄糖利用加速协同所致。对于运动调节骨骼肌的葡萄糖摄取机制已经开展很多研究,但是还是知之甚少。虽然有研究显示CaMK和AMPK在这中间有重要意义,但是其机制还是要进一步研究加以证实。CaMK异构体可能更多地与运动神经元的活动有关,因此被认为是一种前馈调节;而AMPK是在骨骼肌能量状况下降后才被激活,因此被认为是一种后馈调节。PKC、NOS和PKB异构体可能也参与运动所致骨骼肌葡萄糖摄取的调节,但是目前还不能确定。
但是,运动和胰岛素刺激最后都导致GLUT4 转位,这里应该有一种使二者合一的媒介。事实上,aPKC活性在胰岛素刺激和骨骼肌收缩时都会升高,因此目前基本公认这就是使二者合一的媒介。因为运动能提高Ⅱ型糖尿病人的骨骼肌的葡萄糖利用和GLUT4 转位,所以这些信号机制就显得非常重要。因为运动可以在胰岛素抵抗的时候,通过其他的途径提高骨骼肌对葡萄糖的利用。事实上,一些可以激活骨骼肌AMPK活性的药物(如甲福明二甲双胍)就已经被广泛用于治疗Ⅱ型糖尿病。
运动过程中骨骼肌对葡萄糖的摄取主要受到血液运送葡萄糖的速率、肌细胞膜对葡萄糖的转运速率和肌细胞内葡萄糖的磷酸化三个因素的影响,其中,细胞膜对葡萄糖的转运显得尤为重要。运动时细胞内的一些信号分子(如:CaMK,PKC,NO,AMPK,PKB和aPKC等)的变化导致GLUT4转位的增加从而提高肌细胞的葡萄糖转运能力是运动时骨骼肌摄取血液葡萄糖增加的关键所在。
[1] Wright DC,Hucker KA,Holloszy JO,et al. Ca 2+ and AMPK both mediate stimulation of glucosetransport by muscle contractions [J]. Diabetes,2004,53:330 -335.
[2] Terada S,Muraoka I,Tabata I. Changes in [Ca 2+ ]i induced by several glucose transport enhancing stimuli in rat epitrochlearis muscle [J]. J Appl Physiol,2003,94:1813 -1820.
[3] Lee AD,Gulve EA,Chen M,et al. Effects of Ca 2+ ionophore ionomycin on insulin -stimulated and basal glucose transport in muscle [J]. Am J Physiol Regul Integr Comp Physiol,1995,268:R997 - R1002.
[4] Wright DC,Geiger PC,Holloszy JO,et al. Contraction and hypoxia stimulated glucose transport is mediated by a Ca 2+ dependent mechanism in slow twitch rat soleus muscle [J]. Am J Physiol Endocrinol Metab,2005,18 (1).