




解吸是分子或原子离开表面的过程。根据吸附质-吸附剂键的性质和用于打断它的能量形式,存在多种解吸机制。这些解吸机制对于刻蚀非常重要。
在热解吸的情况下,解吸速率是表面温度的函数。固态材料的温度是固体中原子振动能量的量度。原子的能量并不都相等,它们遵循某种分布。原子振动与声波有关,在量子力学粒子表示法中称为声子。例如,非相互作用量子力学声子的能量遵循玻色-爱因斯坦统计分布。能量分布的存在表明,对于给定的温度,存储在键的振动中的能量有可能导致其断裂。键能越低,键被打断的概率越大。通过弱范德瓦尔斯键或氢键(键能通常在10~100meV范围内)结合到表面的原子将在比化学吸附的原子或分子解吸低得多的温度下解吸,后者原子或分子与表面形成更强的共价键(键能通常在1eV左右)。这就是为什么物理吸附发生在相对较低的温度下。当原子的振动能随着表面温度的升高而增加时,从统计学上讲,最弱的键将首先断裂。在均质材料中,所有键都是相似的,因此,体材料将在足够高的温度下升华。
化学吸附削弱了表面与体区的键。这是因为原子之间共价键的强度与共价电子位于这些原子之间的概率成正比。因此,与表面原子结合的吸附质通过改变电子密度来削弱其与表面的结合。这可能导致图2.1所示的情况。提高温度将在比均质体材料更低的温度下破坏表面和体原子之间的键。结果,只有固体材料的顶层被去除。因此,化学吸附通过热解吸实现化学辅助刻蚀,如图2.5中的Lennard-Jones图所示。一条新的Lennard-Jones势能曲线添加到其中,用虚线表示,以表示新形成的分子的势能,该分子包含至少一个表面原子和另一表面原子。
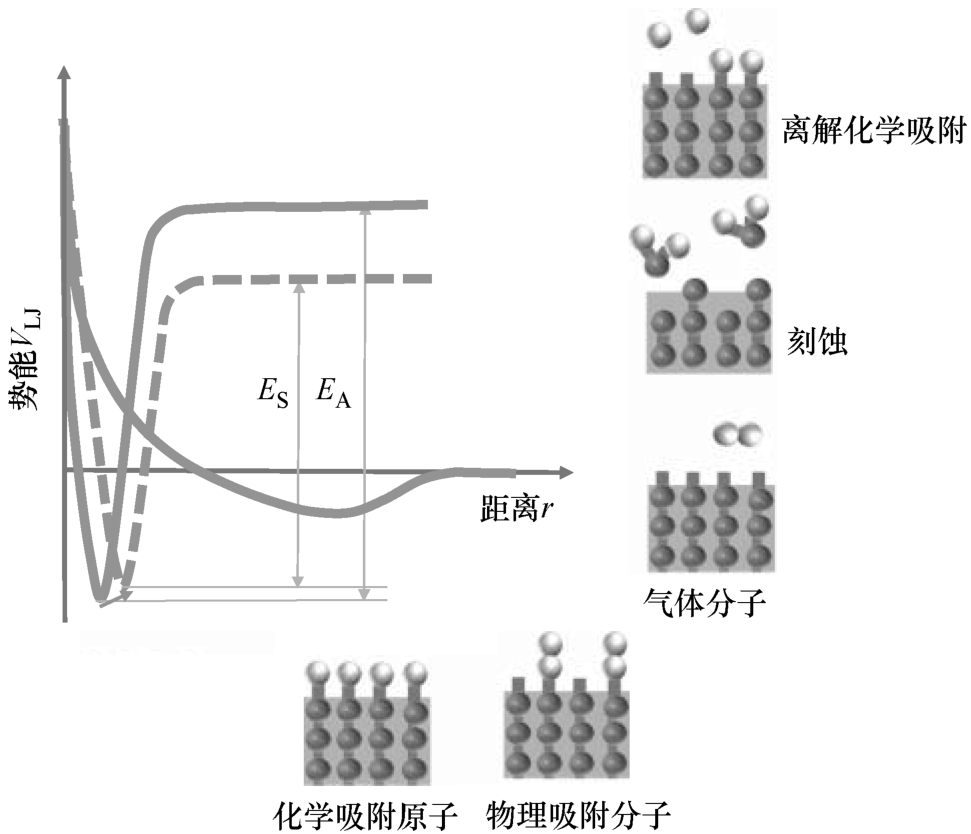
图2.5 热刻蚀的Lennard-Jones图
解吸速率可用阿伦尼乌斯方程描述:

式中, R D 是解吸或刻蚀速率; E a,D 是解吸或刻蚀的活化能。活化能 E a,D 分别与解吸和热刻蚀的吸附能 E A 和表面能 E S 相关。 E a,D 考虑了反应动力学和相应的能量势垒,而 E A 和 E S 仅表示生成焓,没有考虑活化势垒(见图2.4)。当然,这是一个非常简化的表示。