




选择性门静脉栓塞(portal vein embolization,PVE)及门静脉结扎(portal vein ligation,PVL)已被证实是一种安全有效促进门静脉血流、保留供应侧肝叶代偿增生的方法 [1,2] 。1920年Rous P和Larimore LD报道在兔模型上结扎门静脉支后,门静脉阻塞侧肝段进行性萎缩、而通畅侧肝段发生了增生 [3] 。1982年,Makuuchi M将PVE作为辅助技术引入到大范围肝切除的术前准备,并于1984年首先将PVE技术应用于肝门部胆管癌的术前准备 [4] 。此后PVE技术在临床上逐渐广泛应用。
2014年Shindoh J等发布了MD Anderson Cancer Center一项持续18年、包括结肠癌肝转移、肝细胞肝癌、肝外或肝内胆管癌、神经内分泌肿瘤等的临床治疗研究报道 [5] ,在拟行“大范围计划性肝切除(planned major or extended hepatectomy)”病例中,术前评估当拟残余肝体积无法满足以下条件时:正常肝脏者不少于20%、术前已进行全身化疗或病理证实已有肝组织损伤者不少于30%及慢性肝病不少于40%,有358例患者进行了术前PVE准备(其中235例行门静脉右支和第Ⅳ段门静脉支联合栓塞的选择性PVE)。该研究表明PVE技术成熟、成功率较高(97.8%),PVE术后中位时间32天时拟残余肝脏中位增生率达50.3%(27.0%~77.8%),PVE术后并发症率(3.9%)及二期手术后90天内因肝衰竭导致的死亡率低(3.8%)。虽因肿瘤进展导致PVE术后有44例(12.6%)患者未能完成二期手术,但作者认为肿瘤进展主要为肝外转移、并无证据表明与未及时一期切除肝内肿瘤有关,PVE是一种安全有效的、能够显著降低大范围肝切除风险的术前准备手段 [5] 。
编者团队围绕PVE在肝胆外科的临床应用也开展了系列研究。我们早期的研究数据表明,对16例肝门部胆管癌患者术前实施PVE,术后2周非栓塞肝叶/全肝体积比较PVE术前增加 3.3%±2.6%,肝增生的速度为(5.1±2.7)cm 3 /d [6] ;我们对 7 例中央型肝内外胆管囊肿实施计划性肝切除的临床研究发现,选择性PVE术后3周,非门静脉栓塞的拟保留肝叶体积,由术前的41.0%±8.7%增至51.0%±10.0%,拟保留肝叶增生效果明显,能够保障二期半肝及扩大半肝的大范围肝切除顺利实施 [7] 。此外,编者团队对29例原发性巨大肝癌计划性肝切除的临床研究表明,TACE联合PVE治疗2~4周后有19例患者拟残留肝明显增大、得以顺利实施二期肝切除手术,拟残留肝由PVE术前(395.4±58.7)cm 3 增至(599.2±75.2)cm 3 。虽然乙肝、肝硬化的患者实施PVE后,全肝体积变化无统计学差异(1 249.5cm 3 ±137.3cm 3 vs 1 240.7cm 3 ±149.1cm 3 ),但拟残留肝 /全肝体积比由 31.8%±2.9% 增加至 46.0%±2.4%,统计学分析差异具有显著意义;与有肝硬化背景的患者比较,无肝硬化患者非门静脉栓塞肝叶再生更为明显,其拟保留肝叶/全肝体积比由PVE术前的26.4%±1.1%增加至48.0%±5.5% [8] 。
通过上述研究,编者发现,虽然从增生数据直观显现PVE术后肝再生速率相对ALPPS可能较慢,但编者认为选择性肝叶门静脉分流术后肝叶功能的转移是其重要机制,近期的一项研究结果支持编者这一临床实践体会。对90例门静脉右支栓塞病例术后通过 99m -mebrofenin进行肝胆系统显影并计算肝功能响应率和体积响应率,发现门静脉栓塞术后3周增生肝叶的功能反应超过容积反应 [9] 。此外,编者认为,大范围肝切除后剩余肝脏门静脉压力在短期内迅速升高 [10,11] ,亦是术后发生肝衰竭的重要血流动力学机制,术前PVE/PVL能够为预保留肝叶提供充分的血流动力学改变预适应时间。因此,对拟实施大范围肝切除的患者术前进行PVE或PVL,对防范术后发生肝衰竭具有多重保护机制,具有积极的临床意义。
PVE栓塞材料多样,包括弹簧微钢圈、明胶微球、吸收性明胶海绵、凝血酶、超乳化碘油、纤维蛋白胶、无水乙醇、聚乙烯醇颗粒、氰基丙烯酸正丁酯(N-Butyl cyanoacrylate,NBCA)等,多种材料个体化联合应用能够增强栓塞效果(图2-5-1)。
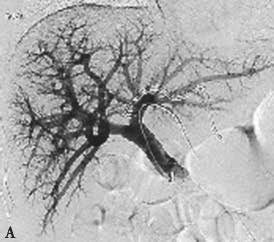
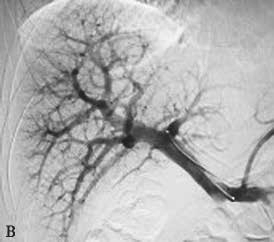
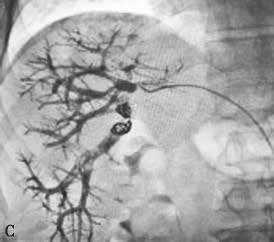
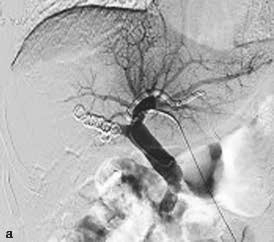
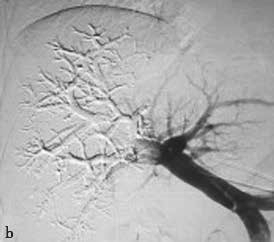
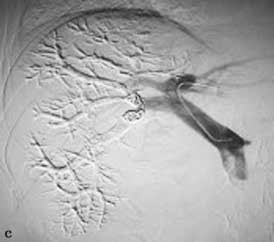
图2-5-1 采用不同栓塞材料实施PVE
A、a.弹簧微钢圈栓塞门静脉右支;
B、b.氰基丙烯酸正丁酯栓塞门静脉右支和Ⅳ段支;
C、c.微钢圈联合氰基丙烯酸正丁酯栓塞门静脉右支。
PVE术后需警惕的并发症包括肝穿刺点出血、胆漏。此外,需警惕术后钢圈等栓塞材料移位导致栓塞对侧门静脉分支或主干栓塞(图2-5-2)。
PVE术后应常规监测门静脉血供,了解选择性门静脉栓塞支血管是否再通,是否发生其他门静脉分支血栓等情况,必要时可选用合适的栓塞材料或无水乙醇进行靶血管的再次栓塞。
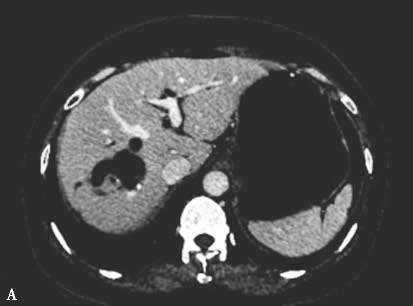
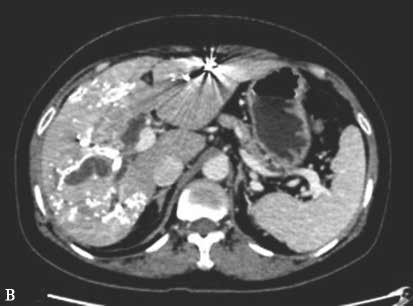
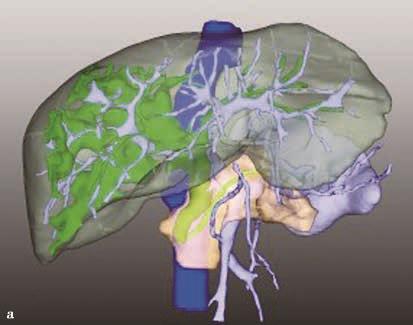
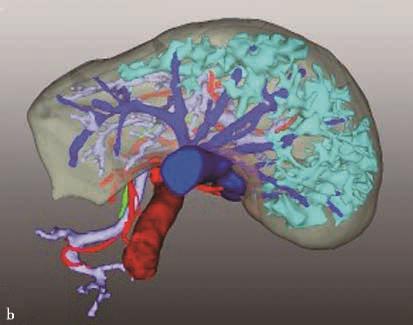
图2-5-2 选择性门静脉右支栓塞,栓塞材料移位至门静脉左支
A.PVE术前CT;a.PVE术前三维可视化重建;
B.门静脉右支行弹簧微钢圈联合NCBA栓塞,术后2周复查CT见弹簧微钢圈移位至肝左外叶门静脉末梢支,肝左内叶见NCBA分布;b.PVE术后三维可视化重建,NCBA自门静脉右支移位至门静脉左内叶分支。
对于非肿瘤性胆道疾病,例如肝内胆管结石、先天性胆管囊状扩张症,可根据肝功能评估结果、肝切除范围个体化制订选择性PVE/PVL术前准备方案。制订PVE的术前准备方案,应在明确肝切除术能够完整切除病灶的原则下实施。双侧肝内胆管结石广泛分布、联合肝切除术无法取尽结石者;因长期肝内结石已发生“肝叶萎缩-增大综合征”者;Todani Ⅴ型双侧肝内胆管囊状扩张症(Caroli病)的患者,不具有实施选择性PVE/PVL的指征。
对于胆道肿瘤患者,选择性PVE/PVL适用于疾病进程相对缓慢的肝门部胆管癌的大范围肝切除术前准备(图2-5-2)。由于胆囊癌、肝内胆管癌病情往往进展迅速,实施选择性PVE/PVL的决策应慎重考量,必要时应在联合放射治疗、控制病灶发展的措施下,酌情实施。实施选择性PVE时,应避免在肿瘤侧肝叶实施穿刺、防止肿瘤细胞随针道转移。
此外,实施选择性PVE/PVL方案前,应详细了解肝功能、门静脉血管解剖影像,并精确测量各目标肝叶体积,以做到栓塞或结扎目标肝叶的门静脉支确实可靠,避免因门静脉分支解剖异常导致栓塞、结扎失误造成严重并发症,或栓塞后拟残留肝叶代偿增生未达到预期效果。
PVE术前及术后需动态测算肝脏体积及拟残留肝体积。计算患者拟残留肝体积与体重比,是临床传统的测算人体必需肝实质体积的方法,当比值大于0.8%提示拟残留肝或受体移植供肝体积能够发挥必要的肝功能 [12] 。目前多通过测算拟残留肝体积与全肝体积的方法进行评估。目前临床上有多种标准肝体积计算公式,国际上应用较多的有Urata公式 [13] 和Vauthey公式 [14] 。香港大学范上达团队 [15] 及四川大学严律南团队 [16] 分别针对中国香港和内地地区人群,建立了标准肝体积计算公式(表2-5-1)。随着肝脏三维可视化技术的成熟,利用肝脏三维成像直接测量全肝体积和拟残留肝体积,可在PVE术前及术后精准动态评估各项数据,有助于制订更为个体化的肝切除方案。
表2-5-1 标准肝体积计算公式

注:BSA:body surface area,体表面积;BW:body weight,体重。
编者建议可参照拟残留肝体积/全肝体积比和肝储备功能,联合制订PVE的适应证 [11,12,17,18] :
具有慢性病毒性肝炎、肝硬化、脂肪性肝炎等肝脏基础疾病者:合并梗阻性黄疸,对拟残留肝叶胆道引流后可实施PVE;无黄疸及拟残留肝叶胆管扩张且ICG-R15=10%~20%,应实施PVE。
无上述肝脏基础疾病且ICG-R15<10%,应实施PVE。
[1]MAKUUCHI M,THAI B L,TAKAYASU K,et al.Preoperative portal embolization to increase safety of major hepatectomy for hilar bile duct carcinoma:a preliminary report[J].Surgery,1990,107(5):521-527.
[2]CAPUSSOTTI L,MURATORE A,BARACCHI F,et al.Portal vein ligation as an efficient method of increasing the future liver remnant volume in the surgical treatment of colorectal metastases[J].Arch Surg,2008,143(10):978-982.
[3]ROUS P,LARIMORE L D.Relation of the portal blood to liver maintenance:a demonstration of liver atrophy conditonal on compensation[J].J Exp Med,1920,31(5):609-632.
[4]MAKUUCHI M,TAKAYASU K,TAKUMA T,et al.Preoperative transcatheter embolization of the portal venous branch for patients receiving extended lobectomy due to the bile duct carcinoma[J].J Jpn Soc Clin Surg,1984,45(12):1558-1564.
[5]SHINDOH J,TZENG C W,ALOIA T A,et al.Safety and efficacy of portal vein embolization before planned major or extended he-patectomy:an institutional experience of 358 patients[J].J Gastrointest Surg,2014,18(1):45-51.
[6]易滨,徐爱民,姜小清,等.肝门部胆管癌术前行门静脉栓塞16例分析[J].中国实用外科杂志,2010,30(6):477-479.
[7]李斌,邱智泉,姜小清,等.计划性肝切除在“中央型”肝内外胆管囊肿治疗中的应用[J].中华肝胆外科杂志,2017,23(9):619-623.
[8]袁磊,罗贤武,姜小清,等.术前序贯肝动脉化疗栓塞联合门静脉栓塞在临界肝切除肝癌治疗中的应用[J].中华肝胆外科杂志,2017,23(10):649-654.
[9]RASSAM F,OLTHOF P B,VAN LIENDEN K P,et al.Functional and volumetric assessment of liver segments after portal vein embolization:differences in hypertrophy response[J].Surgery,2019,165(4):686-695.
[10]CARRAPITA J G,ROCHA C,DONATO H,et al.Portal venous pressure variation during hepatectomy:a prospective study[J].Acta Med Port,2019,28;32(6):420-426.
[11]RYU T H,JUNG J Y,CHOI D L,et al.Optimal central venous pressure during the neohepatic phase to decrease peak portal vein flow velocity for the prevention of portal hyperperfusion in patients undergoing living donor liver transplantation[J].Transplant Proc,2015,47(4):1194-1198.
[12]DELAND F H,NORTH W A.Relationship between Iiver size and body size[J].Radiology,1968,191(6):1195-1198.
[13]URATA K,KAWASAKI S,MATSUNAMI H,et al.Calculation of child and adult standard liver volume for liver transplantation[J].Hepatology,1995,21(5):1317-1321.
[14]VAUTHEY J N,ABDALLA E K,DOHERTY D A,et al.Body surface area and body weight predict total liver volume in Western adults[J].Liver Transpl,2002,8(3):233-240.
[15]CHAN S C,LIU C L,LO C M,et al.Estimating liver weight of adults by body weight and gender[J].World J Gastroenterol,2006,14;12(14):2217-2222.
[16]李富贵,严律南,李波,等.中国成人标准肝体积评估公式的临床研究[J].四川大学学报(医学版),2009,40(2):302-306.
[17]SEYAMA Y,KUBOTA K,SANO K,et al.Long-term outcome of extended hemihepatectomy for hilar bile duct cancer with no mortality and high survival rate[J].Ann Surg,2003,238(1):73-83.
[18]易滨,姜小清.肝门部胆管癌的计划性肝切除[J].中国普外基础与临床杂志,2011,18(6):576-578.