




急性肾小球肾炎(acute glomerulonephritis),又称急性感染后肾小球肾炎,简称“急性肾炎”。多数患者存在前驱感染,其中最典型的疾病为急性链球菌感染后肾小球肾炎。其他如金黄色葡萄球菌感染所致感染后肾小球肾炎相对少见。本节主要介绍急性链球菌感染后肾小球肾炎。
急性肾小球肾炎多见于儿童和青少年,常见的前驱链球菌感染为急性扁桃体炎、猩红热和脓疱疮。一般感染后潜伏期1~3周,起病急,多表现为急性肾炎综合征,即血尿(可为肉眼血尿)、蛋白尿(可表现为肾病综合征)、水肿、高血压,少数患者伴发一过性AKI。部分患者可无明显临床症状,也有少数患者临床表现为急进性肾小球肾炎。多数患者发病时补体C3下降,6~8周恢复正常。肾脏病理学表现为毛细血管内增生性肾小球肾炎。该病具有自限性,治疗以支持和对症为主。如仍存在感染灶,可予抗生素治疗。
既往认为该病预后良好。近年研究显示成年患者、有合并症的患者预后相对较差,可遗留CKD。
门诊病历摘要
患者,男性,14岁,初中学生。因“尿色加深1d伴水肿”入院。患者1d前发现尿色加深,尿中泡沫多,伴眼睑和双下肢水肿,无尿频、尿急和尿痛,无发热。追问病史,患者2周前咽痛、发热(体温38.5°C),应用阿莫西林胶囊1d后热退,抗生素疗程5d,咽痛好转。自发病以来体重增加5kg。既往体健,否认家族肾脏病病史,否认食物和药物过敏史。
突然出现尿色加深,问诊和体格检查时应注意什么?
尿色加深应明确是否为真性血尿。首先需要除外摄入特殊食物和药物所致。进食某些食物(如胡萝卜)和药物(如利福平、卡巴克洛)可有红色尿。确认血尿后还应排除其他脏器出血混入尿液(如女性患者应了解月经史),或者系统性疾病出血(如凝血功能和/或血小板功能障碍等)可能。
鉴别内科或外科血尿。应询问是否有外伤史、泌尿系统疾病病史或有创性检查,外科相关血尿可伴有泌尿系相关部位疼痛、尿路刺激征等症状,尿中可见血丝或者血块;肾小球肾炎所致的血尿多为全程血尿,可伴有长时间不易消散的泡沫。
体格检查时应重点检查患者可能存在的感染源,如扁桃体是否仍存在感染征象、水肿部位、是否存在肾区叩击痛。此外,需要注意是否有皮疹。
知识点
尿色加深需要排除食物和药物所致,确认血尿后需要鉴别内科或外科源性血尿。
入院体格检查
体温36.7°C,心率90次/min,血压145/90mmHg,体重60kg。全身皮肤未见皮疹和出血点。咽红,双侧扁桃体无肿大。两肺未闻及干、湿啰音。腹平软,未触及包块,双肾区无叩痛。双下肢踝部水肿。
该患者应行哪些实验室和/或影像学及有创检查?
血、尿常规检查可提示是否存在感染和肾炎综合征,尿红细胞位相检查可鉴别血尿来源。尿蛋白定量和肝肾功能、肾脏超声可协助肾炎或肾病的临床诊断,并决定行肾活检的必要性和可能性。免疫球蛋白和补体检查可提示肾小球肾炎的病因和类型。
该患者检查结果:血常规未见异常。尿常规:蛋白1.5g/L,红细胞70~80个/HP,白细胞5~10个/HP。尿红细胞位相:变形性为主,可见面包圈样和棘形红细胞。24h尿蛋白定量2.5g。血清白蛋白35g/L,血清肌酐140µmol/L,血甘油三酯和总胆固醇正常。超声检查双肾形态大小和结构正常。
根据患者的临床表现和初步实验室检查,该患者最可能的诊断是什么?需要哪些进一步的检查?
患者急性起病,临床上表现为血尿、蛋白尿、水肿和高血压,符合急性肾炎综合征。因患者上呼吸道感染2周后发生急性肾炎综合征,最可能是急性感染后肾小球肾炎。需要检查抗链球菌溶血素O、咽拭子、血清补体水平并观察变化趋势,以明确是否罹患急性链球菌感染后肾小球肾炎。患者为青少年,血肌酐轻度升高,合并了AKI。需检测ANCA和抗肾小球基底膜抗体(antiglomerular basement membrane antibody,抗GBM抗体)以除外急进性肾小球肾炎,必要时可行肾活检以明确病理诊断并指导进一步治疗。
知识点
1.链球菌感染可引起典型的急性感染后肾小球肾炎。
2.急性链球菌感染后肾小球肾炎主要表现为急性肾炎综合征。
3.急性链球菌感染后肾小球肾炎血清补体C3可一过性下降。
患者血清抗链球菌溶血素O:1 250IU/ml;咽拭子培养为溶血性链球菌;补体C3 0.29g/L,C4 0.24g/L;血免疫球蛋白IgG 16.4g/L,IgA 3.71g/L,IgM 0.96g/L;自身抗体:抗核抗体(antinuclear antibody,ANA)(-),抗双链DNA(double-stranded DNA,dsDNA)抗体(-),抗可提取性核抗原(extractable nuclear antigen,ENA)抗体(-),ANCA(-),抗GBM抗体(-)。
根据上述结果,患者初步诊断为急性链球菌感染后肾小球肾炎。
急性感染后肾小球肾炎的发病机制有哪些?
阐明急性感染后肾小球肾炎的发病机制有助于理解疾病的发生发展过程,有助于决定治疗策略并判断疾病预后。
存在易感因素(如补体基因)的个体罹患感染时,致病微生物诱发机体免疫反应,沉积在肾脏的免疫复合物激活补体造成免疫炎症反应而致病。引起急性链球菌感染后肾小球肾炎的病原菌主要是A组乙型溶血性链球菌中的“致肾炎菌株(nephritogenic strains)”。可能的致病机制:①细菌抗原直接沉积在肾小球(植入抗原);②循环免疫复合物沉积于肾小球;③肾小球固有成分发生改变,成为自身新抗原;④通过抗原模拟,诱发自身免疫反应。
既往认为针对A组链球菌M蛋白的抗体可能与肾小球的自身抗原存在交叉反应,近年研究又认为致肾炎菌株的纤溶酶受体(nephritis-associated plasmin receptor,NAPlr)及链球菌致热外毒素B(streptococcal exotoxin B,SPE-B)是主要的致病抗原。
该患者发病时循环补体C3下降,而C4正常,说明该病主要激活补体旁路途径导致补体消耗。典型的急性链球菌感染后肾小球肾炎血清C3在6~8周恢复正常。
急性链球菌感染后肾小球肾炎是否需要肾活检?典型的肾脏病理学特点是什么?
肾脏病理诊断对于该病确诊是非常重要的。但是对于儿童患者,特别是典型的急性链球菌感染后肾小球肾炎者,可先支持对症治疗。患者临床症状逐步好转,血清补体C3在6~8周内恢复正常,血尿和蛋白尿消失,或仅遗留镜下血尿者可不行肾活检。下列患者应及时肾活检以明确诊断:成人患者或诊断存疑;儿童患者合并AKI;补体C3下降6~8周不恢复;血尿蛋白尿逾期不减少,甚至出现肉眼血尿等。
该患者入院时表现为急性肾炎综合征合并AKI,入院第3日经对症处理并控制血压后行肾活检。
肾脏病理结果:免疫荧光表现为IgG和补体C3呈“满天星”样沿肾小球毛细血管袢和系膜区沉积。光学显微镜检查见肾小球饱满,弥漫性肾小球毛细血管内皮细胞增生,管腔内可见中性粒细胞和单核细胞浸润。电子显微镜检查可见“驼峰状”电子致密物在肾小球上皮下沉积(图3-2-1)。符合急性链球菌感染后肾小球肾炎的病理特点。最终病理诊断为急性毛细血管内增生性肾小球肾炎。
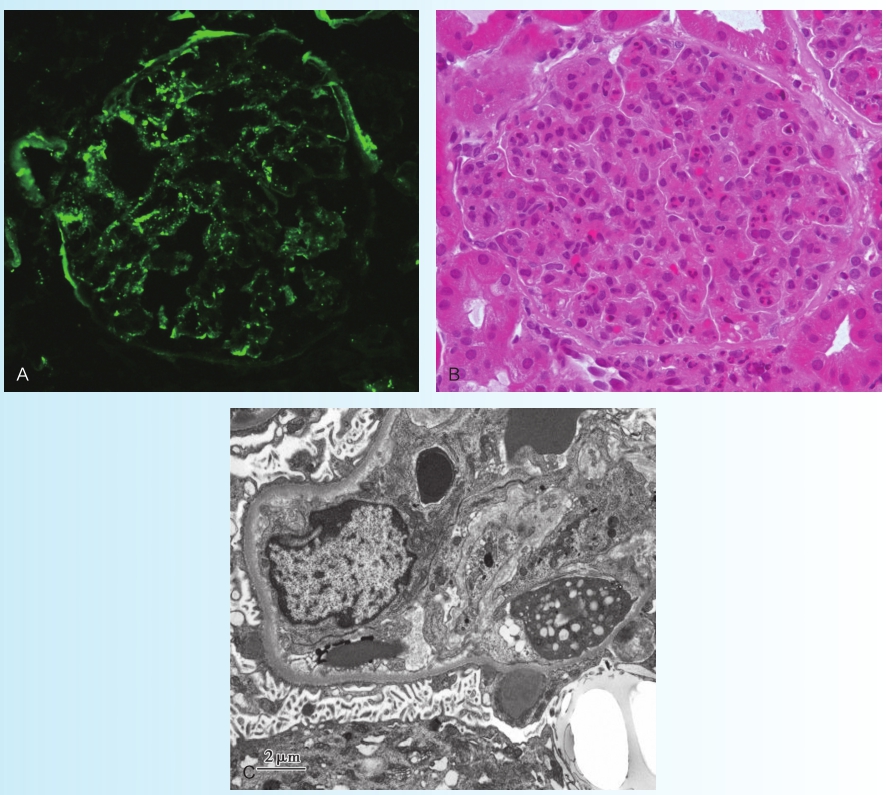
图3-2-1 病理检查
A.免疫荧光示C3呈“满天星”样沿肾小球毛细血管袢和系膜区沉积(×400);B.光镜显示毛细血管内增生性肾小球肾炎(HE染色,×400);C.电镜显示上皮下“驼峰状”电子致密物(×400)。
知识点
急性链球菌感染后肾小球肾炎典型的肾脏病理表现:
1.光镜表现为毛细血管内增生性肾小球肾炎。
2.免疫荧光为IgG和C3呈“满天星”样沿肾小球毛细血管袢和系膜区沉积。
3.电镜可见上皮下“驼峰状”电子致密物。
急性感染后肾小球肾炎的鉴别诊断有哪些?
需要鉴别的疾病包括继发性肾小球疾病,如过敏性紫癜性肾炎,乙型肝炎病毒(hepatitis B virus,HBV)相关性肾炎和狼疮性肾炎等,以及其他原发性肾小球疾病,如IgA肾病和急进性肾小球肾炎等。
1.过敏性紫癜性肾炎
儿童好发,通常合并过敏性紫癜的其他临床表现(包括皮肤型、胃肠型及关节型紫癜)或有紫癜病史,一般无补体水平降低。肾活检可见肾小球系膜区IgA沉积,病理表现与IgA肾病相似。
2.HBV相关性肾炎
该病患者可以出现肾炎综合征、肾病综合征等表现。临床上可有HBV感染的血清学证据和/或HBV-DNA复制证据,肾脏病理学可有HBV相关抗原在肾脏沉积的证据。
3.狼疮性肾炎
好发于中青年女性,多系统受累,实验室检查可见ANA、抗dsDNA抗体和抗Sm抗体阳性。补体C3和补体C4均可降低,随病情活动性变化而波动。肾活检免疫病理检查可呈现多种免疫球蛋白和补体成分沉积,即“满堂亮”的表现。
4.IgA
肾病 中国人最常见的肾小球疾病之一,常表现为急性或慢性肾炎综合征。潜伏期相对较短,可在黏膜感染后数小时至数日内出现血尿、蛋白尿,约1/3的患者血IgA水平升高。肾活检以肾小球系膜细胞增生为主,免疫荧光表现主要为IgA和补体在系膜区沉积。
5.急进性肾小球肾炎
可存在前驱感染,起病急,短期内尿量减少,肾功能进行性减退,多数患者血清ANCA和/或抗GBM抗体阳性。肾活检可见50%以上的肾小球有大新月体形成。
根据目前的诊断,治疗原则是什么?
急性链球菌感染后肾小球肾炎的治疗包括一般/支持治疗、对症治疗和抗感染治疗。
1.一般治疗
(1)卧床休息:
水肿消失、一般情况好转后,逐步增加活动。
(2)饮食治疗:
低盐饮食(<3g/d);优质蛋白饮食0.8~1.0g/(kg·d);热量摄入达到30~35kcal/(kg·d)。
2.对症治疗
(1)利尿消肿:
可应用噻嗪类或袢利尿剂,逐步增加剂量。严重水钠潴留者或发生心力衰竭和脑水肿者可静脉滴注袢利尿剂。
(2)控制血压:
急性链球菌感染后肾小球肾炎患者出现高血压的主要机制为水钠潴留,因此首选利尿剂控制血压。如降压不能达标,也可选用钙通道阻滞剂,但应注意部分钙通道阻滞剂本身有水钠潴留的副作用。急性期过后遗留蛋白尿患者,可选用ACEI/ARB类药物。
3.抗感染治疗
急性链球菌感染后肾小球肾炎发作时,多数患者感染灶已愈。肾小球肾炎的发生与感染后诱发的免疫复合物沉积和补体活化所致炎症反应相关。此时通常不需要使用抗生素药物治疗,除非患者感染灶持续存在。抗感染治疗还可以防止链球菌感染传播他人。一般多选用青霉素类药物。
4.糖皮质激素和免疫抑制剂
目前没有证据提示糖皮质激素和免疫抑制治疗可以改善急性链球菌感染后肾小球肾炎短期及长期的预后,因此不主张临床应用。但有研究显示其他病原体,例如葡萄球菌感染导致的感染后肾小球肾炎,应用糖皮质激素和免疫抑制治疗可能对预后有改善作用,该结论有待进一步研究证实。
知识点
1.急性链球菌感染后肾小球肾炎的治疗以支持和对症为主。
2.水肿和高血压主要为水钠潴留所致,治疗以利尿为主。
该患者入院应用呋塞米利尿后症状逐渐好转,尿量逐渐增加,达2 000ml/d。入院后2周体重下降3kg。尿镜检红细胞5~10个/HP,24h尿蛋白定量0.5g。血清白蛋白40g/L,血清肌酐86µmol/L,补体C3 0.49g/L,停服降压药物,病情稳定出院。
出院后6周(起病后8周)随访,未诉不适。监测血压110/60mmHg。尿镜检红细胞0~3个/HP,尿蛋白阴性。血清白蛋白48g/L,血清肌酐66µmol/L,补体C3 0.89g/L。
急性链球菌感染后肾小球肾炎患者预后如何?
该患者为少年男性,临床表现为急性肾炎综合征,伴高血压和一过性AKI,以及一过性低补体血症,肾脏病理表现为毛细血管内增生性肾小球肾炎。符合急性链球菌感染后肾小球肾炎的自然病程。经支持对症治疗后疾病完全缓解,肾功能恢复,预后良好。
急性感染后肾小球肾炎的预后相对良好,文献报道92%儿童和60%成人患者可临床完全康复。
1.短期预后
死亡率约1%,主要发生于存在基础疾病的老年患者,死亡原因多为并发心力衰竭、脑病和感染。有报道持续少尿、严重高血压、大量蛋白尿,以及病理有新月体病变者,肾功能恢复缓慢。
2.长期预后
既往报道认为长期预后良好,但近期文献报道5年后仍存在蛋白尿的患者中高达8%的患者可遗留CKD。
(赵明辉)
[1] HUNT E A K, SOMERS M J G. Infection-related glomerulonephritis. Pediatr Clin North Am, 2019, 66 (1): 59.
[2] KANJANABUCH T, KITTIKOWIT W, EIAM-ONG S. An update on acute postinfectious glomerulonephritis worldwide. Nat Rev Nephrol, 2009, 5 (5): 259-269.
[3] NACHMAN P H, JENNETTE J C, FALK R J. Primary glomerular disease//Brenner B M, Rector Jr F C. The kidney. 9th ed. Philadelphia: Saunders W B, 2012: 1136.
[4] NADASDY T, HEBERT L A. Infection-related glomerulonephritis: understanding mechanisms. Semin Nephrol,2011, 31 (4): 369.
[5] ODA T, YOSHIZAWA N, YAMAKAMI K, et al. The role of nephritis-associated plasmin receptor (NAPlr) in glomerulonephritis associated with streptococcal infection. J Biomed Biotechnol, 2012, 2012: 417675.
[6] PAIS P J, KUMP T, GREENBAUM L A. Delay in diagnosis in poststreptococcal glomerulonephritis. J Pediatr,2008, 153 (4): 560.
[7] RODRIGUEZ-ITURE B, MUSSER J M. The current state of poststreptococcal glomerulonephritis. J Am Soc Nephrol,2008, 19 (10): 1855.