




血液系统由血液及造血系统组成,包括外周血血细胞、血浆(含凝血相关因子等)和造血器官(骨髓、胸腺、肝、脾、淋巴结及淋巴组织)。血液系统属于结缔组织的一种,起源于中胚层。其主要功能包含血细胞的生成和调节,营养物、氧和代谢物的输送,凝血及纤维蛋白溶解(简称“纤溶”)等。
又称之为外周血,包括血细胞及血浆。血细胞包括红细胞、白细胞及血小板。血浆由水、各种蛋白质和多肽、电解质及营养物质等多种成分构成。
源自骨髓造血干祖细胞分化发育,存在于外周循环池和贮存池中,通过骨髓血液屏障与骨髓中的各阶段幼稚造血细胞相隔离。生理情况下,血细胞生成和破坏或消耗处于动态平衡状态,维持血细胞计数稳定。
是血液中数量最多的血细胞。形态学上,成熟红细胞形态呈中央薄、周围厚的双凹圆盘形,既扩大胞内外气体交换面积,又具有较强的柔韧性,便于通过微小毛细血管。一旦红细胞形状出现异常,红细胞变形能力减弱,就易发生机械性溶血。血红蛋白是红细胞的主要胞质器,结合与输送氧和二氧化碳,贫血患者因血红蛋白减少,导致全身组织器官缺氧进而产生贫血相关症状。红细胞寿命一般为120d,红细胞寿命缩短,红细胞过早过多破坏的现象均称之为溶血,当溶血超过骨髓造血代偿能力时,即可导致贫血。
外周血白细胞包括中性粒细胞、淋巴细胞、单核细胞、嗜酸性粒细胞和嗜碱性粒细胞,不同种类的白细胞形态与功能各异,主要功能是参与人体对入侵异物的“防御”,介导天然免疫和特异性免疫反应。
中性粒细胞又称中性多形核粒细胞,富含能杀灭微生物的蛋白颗粒和酶,是机体抵抗病原微生物的第一道防线,其主要功能是杀菌或抑菌。从原粒细胞发展到成熟粒细胞需8~14d,随后在外周血中循环6~8h后进入组织,不再返回血液。嗜酸性粒细胞主要功能是参与过敏反应、抗寄生虫等。嗜碱性粒细胞释放组胺等介导过敏反应。
其主要功能是通过吞噬、分泌或释放多种生物活性物质,介导各种病原微生物、衰老组织的识别和清除、杀伤肿瘤细胞,是机体抵御入侵细菌的第二道防线。从原始单核细胞发育为成熟的单核细胞大约需5d,后者在外周血液循环中的半衰期为17.5h,进入血管外组织后分化为各器官特异性巨噬细胞,如肝脏的库普弗细胞、骨骼的破骨细胞等。
是一类异质性细胞群,根据其胞膜标记分为多种淋巴细胞亚群,介导免疫应答,其主要包括T(淋巴)细胞和B(淋巴)细胞。不同淋巴细胞寿命相差很大,几个小时至几年不等。
其主要功能参与生理性止血和血液凝固,维持血管内皮的完整性。是早期止血的关键因素。血小板寿命为9~12d。
凝血相关因子包括促凝因子(又称凝血因子)及抗凝物质。血浆中至少含有16种凝血因子,大多数是在肝脏合成的糖蛋白,只有少数是来自单核细胞、内皮细胞和巨噬细胞。生理情况下,凝血因子以无活性的酶原蛋白形式存在,凝血启动后转化为凝血活性因子,产生局限性血栓。凝血过程由内源或外源凝血系统启动。凝血过程是凝血因子按一定顺序“瀑布式”激活,通过阶梯反应的基本效应由血管损伤启动的微小活化信号迅速放大,最终形成牢固的止血血栓。抗凝物质主要包括抗凝血酶-Ⅲ(AT-Ⅲ)、α 2 -巨球蛋白、肝素辅因子、组织因子途径抑制物(TFPI)等,通过抑制促凝酶限制凝血酶生成,使凝血过程局限在局部。
纤溶系统主要包括纤溶酶原和纤溶酶、纤溶酶原活化物及纤溶系统抑制物,其功能是清除血凝块和维持血管畅通。
外周血中寿命有限的血细胞永不枯竭的根本原因是造血器官中的造血干细胞(hematopoietic stem cell,HSC)源源不断地产生新的血细胞。血细胞的发育是连续过程,根据发育过程中细胞的功能和形态特征,人为划分为3个阶段:多能干细胞池、定向干细胞池、形态学可辨认细胞池。多能干细胞在增殖的同时,具有“自我更新”特性,保持其多向分化能力和永不枯竭;定向干细胞阶段不再具有自我更新能力,只具备增殖、分化与成熟能力。外周血含少量造血干细胞(图1-1-1)。
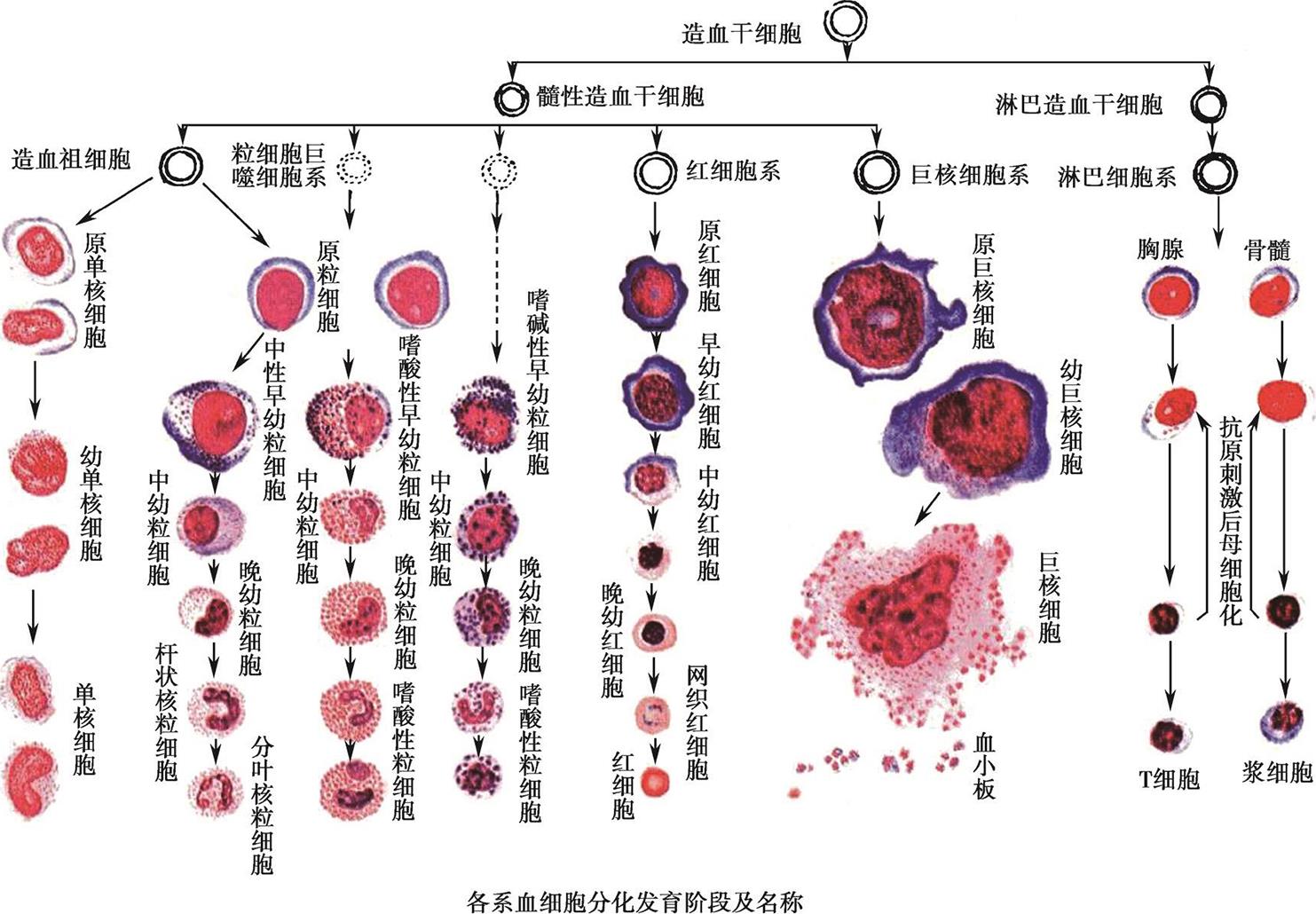
图1-1-1 血细胞发育模式图
人类造血中心从胚胎期到出生后在不同组织和器官转移,人胚第6周起至3~6个月的胚胎,肝脏是造血主要场所,产生红细胞为主;此阶段脾、肾、胸腺和淋巴结等亦逐渐开始具有造血能力,产生淋巴细胞、粒细胞为主,此阶段称为肝造血期。胚胎第5个月后,骨髓造血增加,肝脾等组织造血逐渐减少,骨髓成为造血中心,产生红细胞、粒细胞和巨核细胞等,骨髓是人类终身造血场所,此阶段称为骨髓造血期。婴幼儿期,骨髓腔充满红骨髓,5岁后,长骨骨干骨髓腔中富含脂肪组织的黄骨髓逐渐呈向心性由远端开始替代红骨髓,至成年人,仅不规则骨(胸骨、肋骨、肩胛骨、脊柱、髂骨等)的骨髓腔内仍为红骨髓。
骨髓包括造血细胞及造血微环境(由神经、血管、基质细胞、细胞外基质等组成)。定向造血干细胞逐步分化为红细胞系统、粒细胞系统、巨核细胞系统及淋巴细胞系统的各阶段造血细胞。造血微环境参与造血干细胞的维持、自我更新和定向分化、归巢。造血细胞在骨髓中经过一系列增殖、分化和成熟,发育成具有特定生理功能的终末细胞,穿越骨髓的髓血屏障(marrow-blood barrier,MBB)释放到外周血中。
出生2个月后,肝、脾、淋巴结等不再具有造血功能。但在某些病理情况下,如骨髓纤维化,这些组织又可重新恢复造血功能,称为髓外造血。
骨髓和胸腺又是机体中枢免疫器官,免疫细胞均起源于骨髓的多能干细胞,B细胞在骨髓中发育成熟,参与特异性体液免疫应答,T细胞在胸腺中成熟,参与特异性细胞免疫应答。T细胞、B细胞发育过程均需经过克隆选择,清除自身反应性克隆,产生自身耐受。周围免疫器官包括淋巴结、脾和扁桃体等,是免疫应答的主要场所。
脾脏是主要的淋巴器官,但位于血液循环的通路上,其主要功能是免疫应答、血液滤过及储存。
(邵宗鸿)
[1]YIN A H, MIRAGLIA S, ZANJANI E D, et al. AC133, a novel marker for human hematopoietic stem and progenitor cells. Blood, 1997, 90 (12): 5002-5012.
[2]ZANDSTRA P W, LAUFFENBURGER D A, EAVES C. A ligand-receptor signaling threshold model of stem cell differentiation control: a biologically conserved mechanism applicable to hematopoiesis. Blood, 2000, 96 (4): 1215-1222.
[3]TAICHMAN R S. Blood and bone: two tissues whose fates are intertwined to create the hematopoietic stem-cell niche. Blood, 2005, 105 (7): 2631-2639.
[4]ZHANG J, NIU C, YE L, et al. Identification of the haematopoietic stem cell niche and control of the niche size. Nature, 2003, 425 (6960): 836-841.
[5]GARCÍA-GARCÍA A, DE CASTILLEJO C L, MÉNDEZ-FERRER S. BMSCs and hematopoiesis. Immunol Lett, 2015, 168 (2): 129-135.
[6]CHENG H, SUN G, CHENG T. Hematopoiesis and microenvironment in hematological malignancies. Cell Regen (Lond), 2018, 7 (1): 22-26.
[7]SUN J, RAMOS A, CHAPMAN B, et al. Clonal dynamics of native haematopoiesis. Nature, 2014, 514 (7522): 322-327.