




单组试验目标值法在试验过程中仅设立试验组而不设立平行对照组,通过连续纳入符合要求(即纳入/排除标准)的病例系列并进行相关干预来评估其效果,将获得的效果和目标值之间进行比较,来评价试验干预是否达到了预设的目标。包括选择结局指标,建立目标值,计算样本量,观察疗效以及统计分析五个关键步骤。
为尽量弥补单组目标值非同期对照的设计缺陷,我国医疗器械临床试验设计指导原则建议尽可能采用相对客观、可重复性强的评价指标作为主要评价指标,如死亡、失败等,可以是二分类变量,也可以是连续性变量;研究结局可以有多个,包括主要结局、次要结局以及安全性结局。不建议选择容易受主观因素影响、可重复性差的指标作为主要评价指标,如疼痛评分等。但是中医药疗法本身的优势就是改善症状、提高生活质量,主要还是以主观报告的结局为主,这就在所难免或使用到主观量表作为主要结局指标(但不建议只采用中医量表,避免西医同行难以理解),这就要求开展单组目标值法研究时要充分且明确地定义研究人群,详细说明干预措施的使用方法、频率以及疗程,规定随访时间,以及给出明确的疗效判定标准,以便于找到恰当的目标值与之比较。
目标值所对应的研究人群以及疗效判定标准应当与拟开展的单组试验一致,保持可比性,单一主要结局或者由多个结局指标组成的复合结局就选取一个目标值即可;如果临床研究设置了多个主要结局,而且每个结局都同样重要,此时应当为所有重要的结局指标找到各自对应的目标值。在为结局指标选择目标值时主要有三种方法:
1.客观性能标准(objective performance criteria,OPC) OPC是在既往类似器械的临床研究数据的基础上分析得出,用于主要指标的比较和评价,尤其是安全性,通常是一系列性能的每一个单一指标都有一个标准,所以结局指标通常有多个。必须指出的是,经确认的OPC目前并不多见。OPC通常是在设备技术已经足够成熟的情况下开发的,可以基于公开可用的信息,也可以基于对特定类型设备的所有可用研究的数据综合(meta分析),可以看作具有总体特征的参数。OPC通常来源于权威医学组织、相关标准化组织、医疗器械审评机构发布的文件。随着器械技术和临床技能的提高,OPC可能发生改变,需要对临床数据重新进行分析以获得权威部门的确认。所以,基于OPC的定义和适用范围,它主要用于与同类器械或者成熟技术的比较当中,我们开展中医药的临床研究并不是为了比较是否能够达到目前已有的类似中医药疗法的疗效/安全性,通常是为了与目前的标准治疗作比较,因此OPC不适合作为中医药干预措施的对照。
2.性能目标(performance goal,PG) 在设备技术的开发并不太成熟的情况下,并没有足够的历史数据来开发OPC,此时可以考虑构建PG。PG是指FDA认为基于类似的设备得出的足以作为安全性和/或有效性终点比较的数值(点估计值),也可基于有效性终点的置信区间下限,安全性终点的置信区间上限来设置PG。PG通常用于安全性或者有效性的评价,结局指标通常是安全性的单一指标或者有效性的复合终点结局。如果PG被医学或科学协会或标准组织接受或开发,或在FDA指导文件中描述,则具有更大的有效性。PG需要随时更新,当设备开发日渐成熟或者有足够的历史数据时,可以发展成为OPC。与OPC相比,采用PG的单组设计的临床证据水平更低。PG的实现/未实现不能立即得出试验成功/失败的结论,如果发现异常试验数据时,需要对试验结果进行进一步探讨和论证。由此可见,PG作为目标值也是基于类似产品的历史数据,与OPC一样,也不适用于作为中医药干预措施的对照。
3.客观性能目标(objective performance goal,OPG) 在没有或者很少同类器械的研究数据作为参照的情况下,研究者也可以选取非器械治疗(如目前指南推荐的标准药物治疗)的疗效作为对照,目标值可以来源于标准药物治疗的行业标准,或者所有标准治疗临床研究的meta分析结果(该结果最好能够由一个包含目标器械组和标准治疗组的随机对照试验进行校正,以保证目标器械人群与标准治疗人群的可比性),选取其合并的点估计值或者其单侧置信区间作为目标值。值得一提的是,由于治疗手段的不同,药物治疗的安全性与医疗器械的安全性不具有可比性,因此OPG不作为安全性的性能标准,一般仅用于有效性的研究,也就是验证新医疗器械的有效性能是否达到药物治疗的标准。在评价中医药疗法的疗效时,可以采用OPG作为对照来验证中医中医药干预措施的疗效是否能够达到目前西医标准治疗的效果。
1.主要结局指标为二分类变量 所需的参数包括:单组试验主要结局的预期总体发生率π 1 、为该结局选取的目标值π 0 (OPC,PG或者OPG)、Ⅰ类错误率 α (通常取单侧0.025,以下 α 除非特殊说明均相同)、Ⅱ类错误率 β (通常≤0.2)。
当 π 1 , π 0 不太接近1或0时,可采用近似正态法进行样本量计算,公式为:
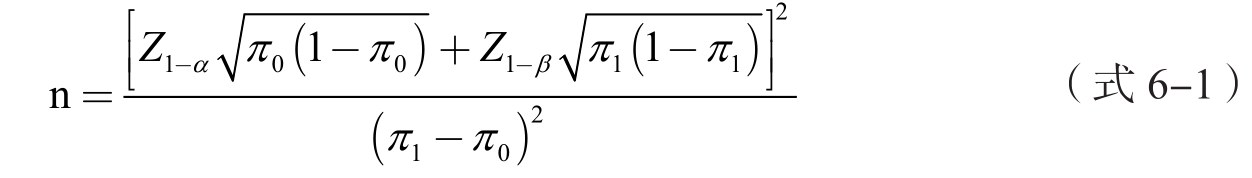
当 π 1 或 π 0 接近0或1时(<0.2或者>0.8),可采用基于二项分布的精确概率法计算,样本量计算公式较复杂且一般情况样本量稍低于近似正态法计算出的样本量,因此也可以采用近似正态法的样本量结果作为参考。
当主要研究终点事件为极小概率或罕见事件时,或终点事件的发生率极高甚至很可能全部发生时,可选用小概率事件的精确概率法进行计算(未考虑把握度,具有较大风险,慎用),公式为:
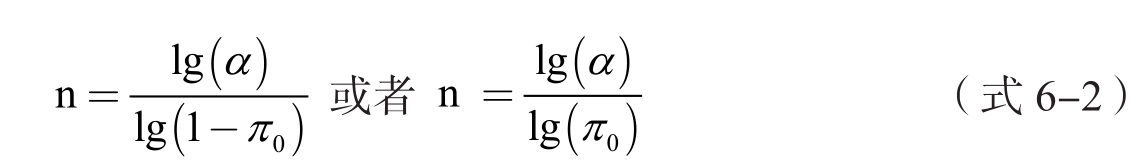
2.主要结局指标为连续型变量 所需的参数包括:单组试验主要结局的预期总体均数μ 1 、为该结局选取的目标值μ 0 、主要结局的预期标准差 σ 、Ⅰ类错误率 α 、Ⅱ类错误率 β 。样本量计算公式为:

需要注意的是,估计的预期总体参数(
π
1
,
μ
1
)一般要优于目标值,即本次单组研究的疗效水平要比目标值高多少才被认为具有临床意义,需要由专业内的专家集体决定。如果临床试验的主要指标数为k个,需要对各指标的把握度进行统一校正,得到每个指标的把握度为
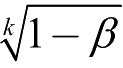 ,据此求得各个主要指标所需的样本量n
j
(j=1,2,…,k),试验的最终样本量确定为所有指标对应样本量n
j
中的最大值max(n
j
)。
,据此求得各个主要指标所需的样本量n
j
(j=1,2,…,k),试验的最终样本量确定为所有指标对应样本量n
j
中的最大值max(n
j
)。
FDA推荐单组目标值法研究主要采用置信区间法进行统计推断,对于主要评价指标,应同时给出全分析集(FAS)和符合方案集(PPS)的统计分析结果。需要计算出单组试验主要终点指标的点估计值和单侧置信区间。在与OPC或者OPG的比较当中,由于OPC和OPG作为目标值时多采用点估计值(即行业内认可的标准),当单组试验结果采用的是高优指标时,要求结局指标的点估计值和单侧置信区间下限均应高于目标值,采用低优指标时点估计值和单侧置信区间上限均应低于目标值,此时可以认为达到了目标值的水平。在与PG比较时,由于PG多选用既往研究点估计值的单侧置信区间作为目标值,这种情况下应该将单组试验的单侧置信区间与所选的作为目标值的单侧置信区间进行比较。也有的研究在使用OPC或者OPG时也采用此两者的单侧置信区间作为其目标值,但这个单侧置信区间需要经过行业内专家和有关部门的认可方可使用。单组试验结果的单侧置信区间估计方法需要根据数据实际情况以及临床情况进行选择。
1.结局指标为二分类变量时单侧置信区间的计算 当样本量n较大,且主要结局的发生率p不太接近1或0时,p的单侧置信区间可采用正态近似法进行估计:
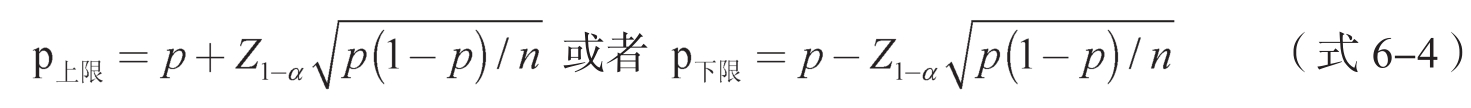
当主要结局的发生率p接近0或1,或n不大时,通常选用二项分布精确法(Clopper-Pearson法)进行估计,如果n例受试者中发生预期结局的例数为x,有效率(高优指标)或者不良事件发生率(低优指标)的100(1-α)%单侧置信区间可用以下公式求得:
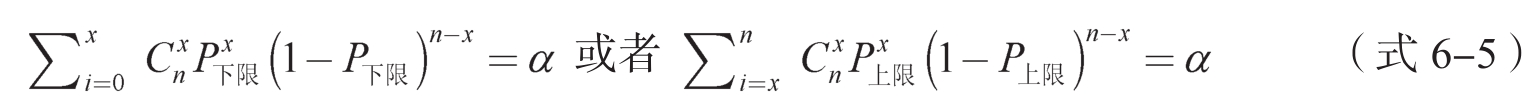
上述公式是基于二项累积分布函数计算,可以通过Beta分布来简化计算过程,经过简化可得如下置信区间计算公式:
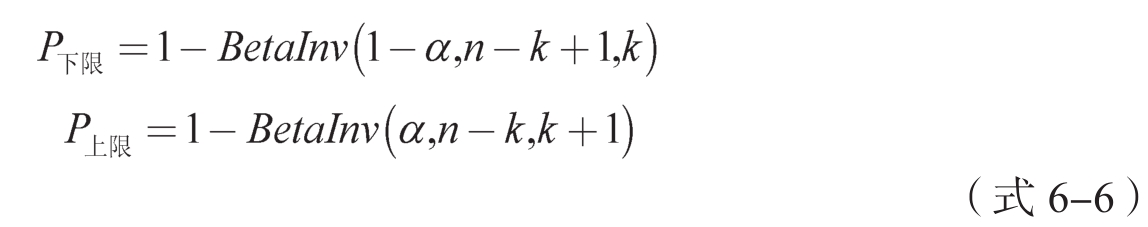
其中 BetaInv ()可以通过 Beta 分布的概率密度函数获得。
2.结局指标为连续型变量时单侧置信区间的计算 当样本量较大时(如n>50),高优指标均值的单侧置信区间下限或者低优指标的上限由下式求得:

当样本量较小时(如n<50),高优指标均值的单侧置信区间下限或者低优指标的上限由下式求得:

当然,也可以采用假设检验的方法进行统计分析,单组试验目标值法研究的假设检验为单侧检验。当 P ≤ α 时( α 取单侧0.025,等同于双侧0.05),拒绝H 0 ,认为干预措施达到了行业标准,即目标值。其统计分析的实质可以看作单组样本代表的总体均数与已知总体的比较,连续变量满足正态分布的情况下可以采用单样本 t 检验,不满足正态分布可以采用符号秩检验,二分类变量可以采用卡方检验的方法进行统计分析,比较单组试验的结果与目标值是否有差异。