




神经元信号活动取决于膜电位的迅速变化。动作电位过程中,膜电位的变化快达500V/s。如此迅速的膜电位变化需通过离子通道(ion channel)才有可能实现。离子通道大多具有传送离子和识别并选择离子种类等重要特性。有一些离子通道总是处于开放状态,允许离子随时出入,不受有关外界信号控制,这些通道属于被动的非门控性通道。但大多数离子通道在电压、化学和机械性信号作用下才处于开放状态,属于主动的门控性通道。电压门控的离子通道至少有2种Na + 通道、4种K + 通道以及3种Ca 2+ 通道(表1-4-1)。新近还发现,通过G-蛋白与受体耦联,从而作为G-蛋白效应器的离子通道。
河豚毒(tetrodotoxin,TTX)和蛤介毒(saxitoxin,STX),可以作为分子探针,以1∶1的形式与Na + 通道结合,测定通道蛋白质。用非离子去垢剂溶解可兴奋膜,可释出Na + 通道。再用色谱技术根据大小、电荷及与碳水化合物共价附着的成分,将糖蛋白分离出来,借以提纯通道。利用这些技术已从电鳗的电器官和哺乳动物的脑和肌肉中提纯了Na + 通道。
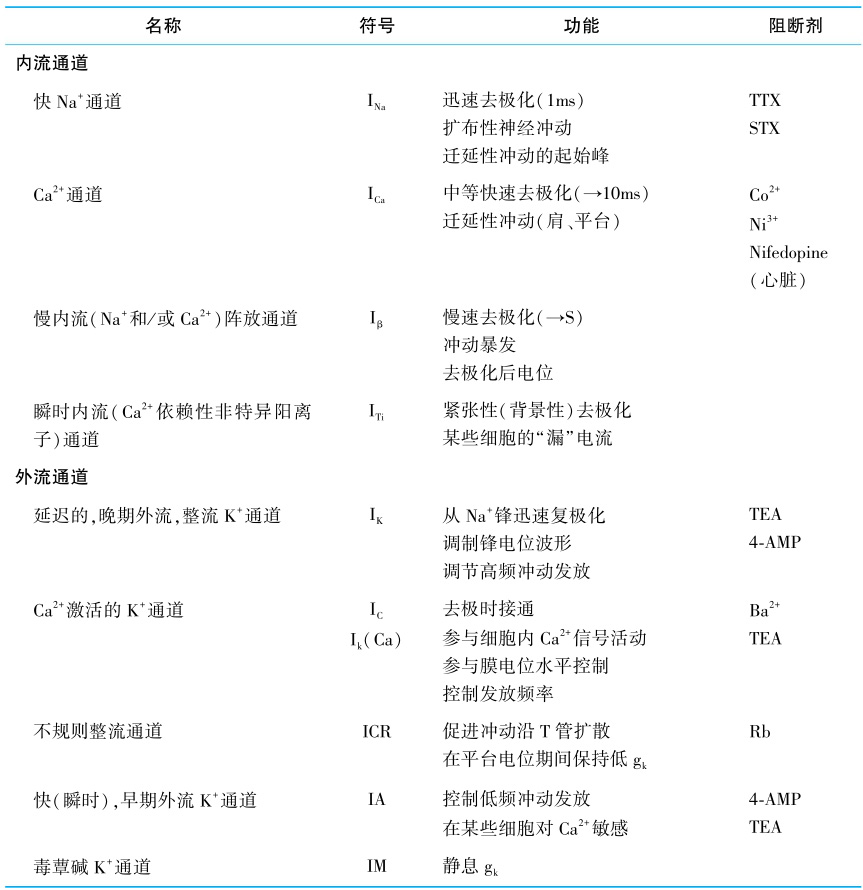
表1-4-1 电压门控离子通道
完整细胞膜与人工提纯的共价标记的Na + 通道的主要成分是分子量为260kD的大糖蛋白。电器官的糖蛋白是唯一的蛋白质成分,但哺乳动物脑的糖蛋白作为α亚单位尚带有两个多肽:β 1 分子量为36kD、β 2 为33kD。脑Na + 通道α亚单位是一种跨膜的多肽,其外表面的位点与碳水化合物链附着,并可与神经毒结合;其细胞内表面上的位点,通过cAMP依赖性蛋白质激酶,进行磷酸化。β 1 和β 2 亚单位因高度糖基化而位于细胞外表面。
β 1 亚单位位置也可靠近与毒素结合的位点,并可被共价标记。β 2 亚单位通过一个二硫键,共价地附着在α亚单位上。β亚单位是膜整合蛋白质,与脂质双层发生相互作用。大α亚单位由1 800~2 000个氨基酸组成,并含有高于50%同源的4个重复的功能区。每一功能区含有300个氨基酸,S 1 ~S 6 等6个节段,形成跨膜的α螺旋。4个功能区由相对亲水的氨基酸序列连接,形成通道壁。
与n-AChR和Na + 通道不同,K + 通道的特异标记毒素尚未被发现。利用分子生物学技术已从果蝇基因组分离出cDNA克隆,证明这种cDNA决定快K + 通道(IA)的多肽结构,可在爪蟾卵母细胞中表达,并显示IA的所有生理学和药理学特性。这种多肽的分子量约为700kD,由616个氨基组成。也具有6或7个跨膜节段,类似Na + 通道4个功能区当中的一个。快K + 通道的120个氨基酸节段(304~435位)有27%与Na + 通道的节段(1 360~1 496位)是同源的。同源区的中心位于Na + 通道中富含精氨酸并参与电压门控的区域,该区域中疏水与亲水残基的交替排列方式也酷似Na + 通道同源功能区的S 4 节段。实际上Ca 2+ 通道的构造也是如此。人们于是开始考虑,快K + 通道在进化上既与Na + 通道又与Ca 2+ 通道有关;但快K + 通道更为古老,可能代表通道的祖代为蛋白质,而Na + 和Ca 2+ 通道则通过基因复制从快K + 通道进化而来。
G蛋白构成一个具有共同构造的大家族,主要影响膜酶活动,进而导致细胞内信息物质(cAMP、cGMP、IP 3 )变化,实现对细胞功能的调节。腺苷酸环化酶(AC)和cGMP、磷酸二酯酶(PDE)等膜酶已被确认为G蛋白的效应器;磷脂酶C(PLC)、磷脂酶A 2 (PLA)和磷脂酰肌醇磷脂看来也是G蛋白的效应器。
电压门控性Na + 、K + 、Ca 2+ 等离子通道均是具有共同结构的大家族成员,也均是G蛋白激活的上述膜酶效应器(AC、cGMP、PDE、PLC或PLA)所生成的胞质信使的下游靶标。但是离子通道同膜酶一样,作为G蛋白效应器的发现也只是近几年的事情。迷走神经释放出的ACh作用到心房肌和心节律细胞上的m-AChR,导致K + 通道开放,使细胞超极化,减慢细胞的节律性去极化。但是,这种膜电位或膜电流变化,在施加乙酰胆碱(ACh)后,需经过一段延搁,才能出现,从而提示m-AChR与K + 通道之间可能需通过G蛋白介导。