





现在说起抗癌进展,最火爆的无疑是免疫疗法。所以这本书里,我也必须专门用一章来介绍乳腺癌中的免疫疗法。
由于概念火热,现在很多疗法都称自己为免疫疗法或者生物疗法。其中靠谱的少,不靠谱的极多。不靠谱的里面,有些是还没有被证明,有夸大宣传的嫌疑,更多的则是纯粹忽悠,新瓶装老酒,把以前不靠谱的东西包装了一下,贴上“免疫疗法”的标签,再次出来招摇撞骗。
我个人觉得,目前对乳腺癌患者而言,真正值得患者关注的免疫疗法主要有下面几种:
1. 抗体靶向药物
2. PD-1/PD-L1抑制剂
3. 肿瘤浸润淋巴细胞疗法
我之所以推荐大家关注,是因为这三类免疫疗法都已经各自在乳腺癌中显示了一定的临床疗效。我们就一起来看看它们的战果吧。
首先是抗体靶向药物。
在乳腺癌里,主要就是针对HER2阳性亚型的大分子靶向药物,比如曲妥珠单抗等。这些药物虽然叫靶向药物,但是起效的原理却和免疫系统密切相关,准确地说,应该叫靶向免疫药物。
曲妥珠单抗是针对癌细胞表面HER2蛋白的抗体,能够紧密地结合癌细胞上。由于一个癌细胞表面有无数的HER2蛋白,因此会结合很多的曲妥珠单抗。从远处看,曲妥珠单抗就像一层衣服一样,盖在了癌细胞上。
这就要出事儿了。
正常细胞表面是不会出现这么多抗体的,所以这种“穿衣服”的细胞显然很不正常。当免疫细胞(自然杀伤细胞、巨噬细胞等)经过的时候,很快就能识别这种穿着奇怪的细胞,并且干掉它(图27)。通过特异的抗体识别,来诱导免疫细胞杀伤特定的癌细胞,这就是曲妥珠单抗这类大分子靶向药起效的重要机制。在专业上,我们称这个现象为“抗体依赖的细胞介导的细胞毒性作用”(antibody-dependent cell-mediated cytotoxicity,ADCC)。
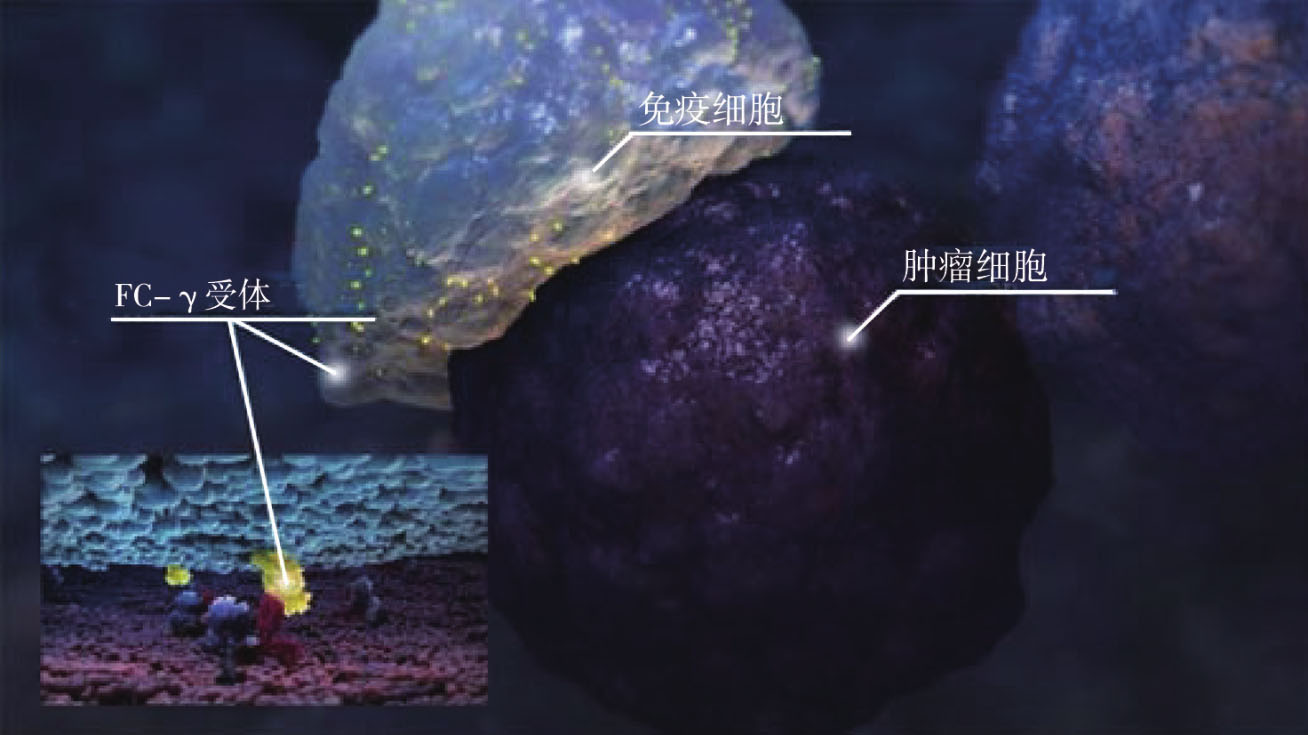
图27 免疫细胞、肿瘤细胞与特异性抗体
好几个重磅的抗癌药都是主要通过ADCC机制来起效的。除了治疗乳腺癌的曲妥珠单抗,还有治疗淋巴瘤的利妥昔单抗(美罗华),以及最近刚在欧美上市的治疗多发性骨髓瘤的新药daratumumab,等等。
ADCC
现在大家说“免疫疗法”,一般就是指PD-1/PD-L1抑制剂这类药物。它们也被称为“免疫检验点抑制剂”。
“免疫检验点”不太好理解,大家可以简单地理解成一个免疫反应的关卡,就像公路检查站一样,告诉免疫系统应该向前攻击目标还是应该打卡下班休息。
免疫检验点是人体自然存在的控制免疫反应的重要临界点,同时有很多激活和抑制的力量在这里进行较量,如果最终激活力量占了上风,免疫系统就被激活,开始清除细胞或病原体;如果抑制力量占了上风,免疫反应就不会被激发。
为什么免疫系统要设立免疫检验点呢?
因为凡事都需要“阴阳平衡”。
生物体的所有系统都是一个通过复杂正反馈和负反馈形成的平衡。正是由于免疫检验点的存在,才保证了免疫系统处在理想状态。如果免疫系统太弱,则容易被感染,容易出现癌细胞,但过犹不及,如果免疫系统被过度激活,就会开始攻击自身正常细胞,产生灾难性后果。很多自身免疫疾病,包括著名的红斑狼疮,就是免疫系统被过度激活的产物。
如果把免疫系统比作一辆汽车,激活正信号就是油门,抑制负信号就像刹车。没有刹车,或者没有油门,都肯定是悲剧的。
PD-1/PD-L1是一条重要的抑制免疫细胞的信号通路,因此深受癌细胞的喜爱。癌细胞显然不愿意被清除,因此想尽各种手段来躲避免疫系统的攻击,其中一个常用办法就是激活PD-1/PD-L1信号通路。当PD-1/PD-L1信号被激活后,免疫系统就收到信号:“这里没事,回去休息吧!”。这种调控PD-1/PD-L1的能力很多正常细胞都有,并不是癌细胞特有的功能,只是有些坏蛋很聪明,“拿来主义”窃取并放大了它的效用。
PD-1/PD-L1抑制剂,比如著名的O药、K药,作用就是解除PD-1/PD-L1对免疫系统的抑制。所谓负负得正,通过抑制一个抑制免疫系统的机制,O药和K药这类药物就能重新启动免疫系统,从而对癌细胞进行攻击。
在十多种癌症类型中,比如黑色素瘤、经典霍奇金淋巴瘤、MSI-H亚型结直肠癌等,这类免疫药物都取得了突破性的进展,让很多晚期无药可治的患者重拾高质量的生活,甚至是重拾整个生命。
乳腺癌也是试验的一个热点。
在各种乳腺癌亚型中,三阴性是目前治疗效果最差、最需要新药的。因此免疫疗法最大的试验田就是在这类患者中。几乎所有的免疫检验点抑制剂都在三阴性乳腺癌中进行过,或者正在进行临床试验。
那这类免疫疗法在乳腺癌中的效果如何呢?
一句话概括:有效果,但单药只是差强人意。
比如默沙东的PD-1抑制剂K药,曾经进行过代号为KEYNOTE-086的一个二期临床试验,专门测试它在三阴乳腺癌中的效果。
如果用于初治患者的一线治疗,整体缓解率(肿瘤明显缩小患者比例)为23%,其中完全缓解率(肿瘤检测不到的患者比例)为4%。这看着还可以。但问题是,如果用于接受过多线化疗的患者,效果就很差了,整体缓解率仅为4.7%,完全缓解率为0.6%。
无独有偶,在另一个免疫药物,罗氏的PD-L1抑制剂阿特珠单抗,在临床试验中也展现了类似的情况。
当用于初诊患者(PD-L1阳性)的时候,整体缓解率为26%,但用于接受过多线治疗患者时,整体缓解率低于10%。
这些数据再次提醒了一点,那就是好药留到最后用不一定是最好的选择,早点用可能效果更佳。从数据来看,无论靶向药,还是免疫药,似乎都是如此。
这并不难理解,由于免疫药物起效需要健康的免疫系统,因此趁患者治疗期短,身体状态好,尤其是免疫系统状态好点儿的时候,早一点开始使用免疫药,或许能达到更好的疗效。
单药效果不理想,咋办呢?
联合用药!
这是最新的一大趋势。很多数据都显示,当免疫疗法结合化疗或放疗,可能产生协同效应,增加效果。
比如,在K药联合化疗药艾日布林的早期研究中,整体缓解率为33.3%,这里面有初治患者,也有经过很多线治疗的患者。从这个数据看,确实比单药更好。
阿特珠单抗也专门在一线患者中做了免疫+化疗联合方案,结果早期临床结果显示,整体缓解率高达70%!最近,公司已经宣布,在三期临床试验(代号为IMpassi on130)中,阿特珠单抗+紫杉醇作为一线治疗取得了成功,延长了患者的总生存期!
这是全球第一个,针对三阴性乳腺癌取得成功的免疫疗法三期临床试验,也期待有更多的好消息。
总之,PD-1/PD-L1类免疫检验点抑制剂目前在乳腺癌治疗中整体缓解率偏低。但在一线治疗组,或者具有明确分子标记特征的患者中,获益更高一些。未来的重点,一方面是寻求更好的组合疗法,另一方面是找到能预测对单药响应患者的标记物。毕竟,能不用化疗就实现缓解是最好不过的了。
最后一种要介绍的免疫疗法,叫作肿瘤浸润淋巴细胞(tumor infiltrating lymphocyte, TIL)疗法。
TIL疗法的原理并不复杂,基本就三步:
1. 取出患者的肿瘤组织,从中提取免疫细胞,主要是T细胞。
2. 在体外筛选能识别癌细胞的T细胞,并且大量扩增到几百亿甚至上千亿个细胞。
3. 把扩增好的细胞输回患者体内,让它们去和癌细胞PK。
说起来简单,但这是一个技术性要求很高的工作,尤其是第一步和第二步,全球没有几个地方能顺利完成。美国国家癌症研究所(National Cancer Institute, NCI)的史蒂文·罗森伯格(Steven Rosenberg)博士是这种技术的先行者和领军人物。
为什么要从患者肿瘤组织里面提取免疫细胞?血液里面不是到处都是免疫细胞吗?
因为不同地方的免疫细胞,识别肿瘤的能力迥异。
大家可能不知道,咱们身体内免疫细胞是有明确分工的,并不是万能型。它们有的识别病毒,有的识别细菌,有的识别肿瘤。这就像一个社会中的人,有各种职业,都很重要,但分工不同。
血液里面分离的免疫细胞,绝大多数都是针对细菌、病毒这些坏蛋的,能识别肿瘤细胞的比例极低,不到0.5%。而肿瘤组织里分离出的免疫细胞,识别肿瘤的比例要高很多。
咱们不是简单地要更多免疫细胞,而是要更多能识别癌细胞的免疫细胞!如果不能识别,再多也是枉然,对患者来说没用。这就像要上战场,光人数多并没有太多用,因为里面可能很多人都晕血,无法打仗。要想打胜仗,关键是要战士多,特种兵更好。
这项技术并不新,从20世纪80年代就已经用在患者身上,主要治疗黑色素瘤,有效率达到50%以上,很多晚期患者能被“临床治愈”。随着科学和临床进步,尤其是基因测序、免疫特异性检测技术,包括其他免疫疗法的成熟,最近它开始在其他癌症类型,包括乳腺癌中展现疗效。
2014年,权威的《科学》杂志上发布了一个案例,一位6个孩子的妈妈美琳达·巴基尼(Melinda Bachini)被诊断为胆管癌,无药可治,结果使用两轮TIL疗法后,肿瘤快速缩小,她几乎恢复了正常的生活。
现在的美琳达,在家照顾3个还未成年的小孩,每天遛狗跑步两英里
 。同时她是“胆管癌研究基金会”的积极倡导者,在世界各地分享自己的故事,鼓励科学家和医生研究罕见癌症,鼓励患者参与临床试验。
。同时她是“胆管癌研究基金会”的积极倡导者,在世界各地分享自己的故事,鼓励科学家和医生研究罕见癌症,鼓励患者参与临床试验。
乳腺癌里也有成功的例子,比如2018年顶尖的《自然·医学》杂志上就发表了一个案例。
现年52岁的工程师朱迪·珀金斯(Judy Perkins),2003年曾因乳腺癌做过乳房切除手术,但在2015年,她体内的癌细胞又复发了,并且转移扩散到了肝脏。
在没有特别好办法的情况下,朱迪选择参与TIL临床试验。
和标准流程一样,研究者首先对患者肿瘤进行了DNA测序,找到了特定的基因突变,同时他们也采集了肿瘤浸润淋巴细胞(TILs)。
通过复杂的分子生物学和细胞生物学试验,科学家找到并提取出了患者体内针对癌细胞的免疫细胞,并且对这些免疫细胞进行了大量扩增。这就是体内抗癌的“特种部队”。
大量的免疫细胞“特种部队”经过体外培养后,重新注入患者体内。为了增加疗效,科学家加入了另外两个能增加抗癌免疫力的药物:白介素2(IL2)和PD-1抑制剂派姆单抗。没错,就是前面我们聊过的免疫检验点抑制剂K药。
这是不折不扣为患者量身订制的免疫疗法,而且是三管齐下。
结果奇迹发生了!
朱迪体内的癌细胞被完全消除,并且截至论文发表的时候,效果已经维持了近两年。朱迪是户外运动爱好者,最近她在美国佛罗里达州完成了一趟近2000千米的极限皮划艇之旅!她的感觉好极了!
毫无疑问,TIL疗法是一个突破,给一些绝望的晚期患者带来了新希望,但它很长时间都处在试验阶段,一直没有办法推广。为什么呢?
除了技术难度很大,很少有人能做以外,还有个重要的问题,那就是TIL疗法有效率比较低。这种治疗方法并不适用于多数患者。
除了黑色素瘤等少见的肿瘤类型,TIL疗法在参与试验的人里面只有15%左右的有效率,目前还无法预测谁会从中获益。
由于TIL疗法是个性疗法,操作复杂,价格很昂贵,如果7个人里面只有1人有效,实在很难上市推广。
无论如何,TIL疗法很值得关注,它不可辩驳地证明了人体内天然存在能对抗癌症的免疫细胞,而且取决于每个人癌细胞突变不同,对抗癌细胞的免疫细胞也都是不一样的。这些结论,对于抗癌的精准医疗,有着非常重要的意义。
未来,我们希望能找到预测TIL疗法效果的生物标记物,同时也需要大力尝试组合疗法,来提高它起效的比例。前面提到的,它和PD-1抑制剂的强强联用,也带来了临床全新的思路,有望帮助更多患者。
总之,各种免疫疗法都在快速推进,也慢慢开始给以前治疗效果不太好的乳腺癌患者带来新的希望。大家有理由保持乐观,保持希望,因为永远不知道下一次突破什么时候就来了!
· 乳腺癌中展示过疗效的免疫疗法包括抗体靶向药物,PD-1/PD-L1抑制剂和肿瘤浸润淋巴细胞疗法等。
· 三阴乳腺癌中单独使用PD-1/PD-L1抑制剂效果不够理想,组合疗法是主流方向。
· 肿瘤浸润淋巴细胞疗法在个别患者身上展示了惊人疗效,但它技术难度大,有效率不够高,目前还没有推广。
