





肾脏发育生物学是研究肾脏的形态发生及发育成熟过程中分子信号调控机制的一门新型交叉学科,发育肾的研究是近年来肾脏病领域的一个研究热点。细胞分子生物学研究显示肾脏损伤和修复过程中出现类似胚胎后肾发育过程的重演,提示肾脏损伤后细胞的再生过程和肾脏胚胎发育过程有着极其密切的关系。对发育肾的研究有助于揭示先天性肾脏发育不良的机制,也有助于理解后天性肾脏疾病发生进展的病理生理机制。
本章将从以下两个方面介绍肾脏的发生和发育过程:
哺乳动物的肾脏起源于间介中胚层体节外侧的细胞索,在胚胎发育过程中重演种系进化的过程,按时间及头尾顺序依次经过前肾(pronephros)、中肾(mesonephros)、后肾(metanephros)三个发育阶段(图1-1),三个阶段遵循相似的发育机制,而且在时空上的发育是连续的,前肾诱导中肾的发生,中肾诱导后肾的发生。前肾和中肾是暂时性的器官,在胚胎发育过程中相继退化,后肾则发育为成年永久性肾脏。

图1-1 胚胎肾脏的发育示意图
胚胎第三周末,随着胚体的卷折,间介中胚层与体节分离,逐渐沿腹侧形成左右两条分列在体节外侧的纵行的索状的生肾索(nephrogenic cord),生肾索的头端(平7~14体节)发育为前肾,胸腹部(平14~28体节)的生肾索,为中肾原基,生肾索的尾端发育为后肾。
人胚胎22天,头端生肾索分节形成7~10对上皮样小管结构,形成纵行的前肾小管(pronephric tubule),前肾小管的外侧端部分向尾侧延伸形成相互连接的纵行上皮性小管,即前肾导管(pronephric duct),除鱼类及两栖动物外,前肾导管在脊柱动物无任何排泄功能。前肾导管出现之后即相继退化。
胚胎24天前肾导管下端向尾侧延伸形成上皮性的中肾导管,即Wolffian导管,其尾端开口于泄殖腔。Wolffian导管和其周围环绕的中胚层肾发生带一起形成中肾。在Wolffian导管诱导下,中肾胚基内形成与Wolffian导管相连的S型中肾小管(mesonephros)和对应的小球结构,小球内有来自背主动脉的毛细血管球,大约先后自上而下可有80对小管样结构,形成过程中,尾侧小管形成后,头侧小管退化,其数目始终维持在15对左右。中肾有一定的排泄功能,之后,中肾小管大部分退化,最后中肾组织演化为生殖系统的发生组织,在人类,男性性腺区域的中肾小管分化成为输精小管,中肾导管分化为附睾及部分输精管。在女性,绝大部分中肾组织退化,部分残留中肾小管形成卵巢及副卵巢。
妊娠28天Wolffian导管尾端近泄殖腔部位,向背侧突出一个上皮性的盲管,称为输尿管芽(ureter bud,UB)。其周围环绕的中胚层间充质称为后肾间充质(mesenchyme),两者构成后肾。在后肾的发育中,两者交互诱导,输尿管芽发育为集合系统,后肾间充质分化发育为肾单位和基质细胞。
成熟的哺乳动物肾脏至少由26种细胞组成,包括上皮细胞、血管内皮细胞、系膜细胞及间质细胞等,目前认为这些肾脏固有细胞主要是由输尿管芽和后肾间充质细胞分化增生而来,输尿管芽和后肾间充质构成肾发生带。
1.集合系统的形态发育
集合系统的形态发育包括一系列相互关联的过程。首先是在后肾间充质的诱导下输尿管芽的形成并侵入后肾间充质,继之侵入后肾间充质输尿管芽的重复分支及衍生出子代集合管,之后皮髓质集合系统的形成,包括输尿管芽分支的再吸收形成肾盂肾盏以及多种上皮细胞的最终分化。
输尿管芽是一个上皮性的盲管,其顶端称为壶腹(ampulla),该部位细胞增殖较快,而其茎干细胞增殖较慢。增殖较快的壶腹扩展延伸,以二叉分支的形式形成两个新的输尿管芽分支,呈“T”型对称分布,其中一支与其诱导形成肾小体连接,另一枝继续以二叉分支的形式分支。在肾脏发育过程中大约可以形成15级分支,最初的2级分支通过再吸收及扩张形成肾盂,3~4级分支形成肾盏和肾乳头,后续的小分支形成集合管,大约共形成65 000条集合管。胚胎3个月,后肾形成了皮髓质分区,开始具有泌尿功能。皮质和髓质集合管两者的形态发生有明显的不同,早期的输尿管芽分支主要位于内髓层,髓质输尿管芽分支较少,集合管相对以无分支的线形延长,而皮质集合管则重复分支并诱导后肾间充质形成肾单位。内髓层输尿管芽分支相对于随后形成的外髓及皮质输尿管芽分支来讲较短而且生长较慢。皮髓质的形成对维持肾脏的功能有着重要的作用。
2.肾单位的形态发育
肾单位(nephron)的形态发育包括:肾小球、肾小管的发生,血管的形成和发育,肾单位的成熟。肾单位起源于后肾间充质,后肾发育的早期,间充质与输尿管芽接触,在其诱导下经历了间充质-上皮转分化,形成极性细胞,分化为肾单位的各个部分。首先是围绕输尿管芽末端的间充质细胞压缩成团,再延长转化为具有上皮样结构的肾囊泡,进入V期;然后肾囊泡拉长、折叠成为comma型小体,进一步变成S型小体,其中S型小体的上支将分化为远端小管并与集合管融合,中间支即成为未来的近端小管,下支或远端部分形成勺状囊样结构,其外侧细胞将发育为肾小球的壁层上皮细胞,其内侧细胞将发育为肾小球的脏层上皮细胞,即足细胞。随之血管球突入勺状囊样结构的靠近中间枝的部位,形成不成熟的肾小球,即毛细血管袢期肾小球(C期肾小球)形成,最终形成成熟的肾小球(M期肾小球)(图1-2)。






图1-2 胚胎8~32周肾脏形态发育
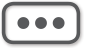
(A)、(B)、(C)和(D)为8~13周胎龄肾组织,(E)为32周龄组织。(A)和(B)可见肾发生带内大量间充质细胞,“T”型输尿管芽末端和肾小球V、S、C期。(C)可见成对C期肾小球,上方为不成熟肾小管。(D)可见M期肾小球和肾小管,其中近端小管显色明显较远端小管为淡。(E)中含有C期肾小球和已出现微绒毛的近端小管。(F)可见成对多代肾小球。其中(m)为间充质细胞,(u)为输尿管芽末端,(v)为肾囊泡,(s)为S型小体,(c)和(M)分别是毛细血管袢期肾小球和成熟肾小球,(pt)和(mt)分别是原始近端小管和成熟近端小管,(dt)代表远端小管
根据不同胎龄输尿管芽和后肾间充质分布情况及各期肾小球分布位置,可明显看出肾发育位置特征,即呈放射状发育,靠近肾髓质中心为成熟肾小球,越近肾包膜越不成熟。在早期肾单位形成过程中,输尿管芽形成“T”型末端,T两侧部位均诱导间充质细胞集中,因此肾小球出现是成对的,说明肾小球数量是由输尿管芽“T”型末端决定的,输尿管芽分支越多最终形成的肾小球也越多。按与分支输尿管芽长轴相垂直的肾小球计数其出现代数,可在一定程度上反映不同时期肾单位发育成熟情况和数量。人类发育中第一个肾小球出现及肾小球形成停止时间,尚有争议,有观察发现8~9周龄胎儿已出现1~2代成熟阶段肾小球和可分辨的近端、远端肾小管,19周已达7~8代,33~34周时为11~12代。从肾发生带消失情况观察,31~32周已明显减少,33~34周消失,提示肾单位分化在33~34周胎龄停止,可能不再有新的肾单位形成,有的学者认为直至孕周的最后一个月,但多数学者认为维持到第34~35周。不同个体最终肾小球数是有差异的,最终成人肾单位的数目约为600 000个。
后肾起初位于盆腔,由于输尿管芽的生长及腔体弯曲度的减小,腰骶部距离增大,使后肾渐上升至腹腔。自第10周起,人类胚胎肾脏开始产生尿液,其产生的尿液进入羊膜腔后与羊水混合,经胎儿消化道吞咽进入胎儿体内,再经肾脏排泄。整个妊娠期间胎儿肾脏基本上不具有排泄废弃物的功能,其排泄代谢废物的功能主要由胎盘替代。胚胎19周之前是肾发育关键时期,任何围产因素都有可能影响肾脏发育,造成肾发育的异常,与成人相比,胎儿成熟期肾小球和肾小管只是相对成熟,还不够完善,如肾小球体积较小、毛细血管袢及开放相对较少、肾小管短粗等,胚胎3 4周后仍需要一个继续发育、完善的过程。
输尿管芽和后肾间充质的交互诱导是肾脏发育的基础和必需的条件,在50年前Grobstein首先阐述了后肾发育依赖于输尿管芽与后肾间充质之间功能上的相互作用。两者交互诱导的过程涉及复杂的基因表达程序,多种转录因子、生长因子和细胞因子、细胞外基质和黏附分子参与其调控。近年来,随着分子生物学实验技术的发展,通过对人类遗传性疾病基因突变分析及动物基因敲除实验的研究和组织细胞培养的方法,进一步阐明了两者交互诱导的分子信号传导机制在肾脏发生分化中的作用。
1.后肾间充质表达因子的调控作用
多种后肾间充质分泌的信号参与输尿管芽发生及分支形成的调控,包括转录因子Wt1、Pax2、Liml以及核蛋白Formin、多肽因子GDNF(glial cell-derived neurotrophic factor,GDNF)等。以上因子可能通过多种途径参与肾发育过程中的分子调控。
2.Pax2-Eya1-Six2-Hoxa11-Foxc1调节途径
Pax2属于同源对子盒基因,是肾脏发育的重要调控因子。肾脏发育过程中Pax2表达于Wolffian导管、输尿管芽、集合管、未被诱导的后肾间充质、压缩间充质、comma小体,其在S小体的表达下降,仅表达于邻近分支输尿管芽的部位,成熟肾单位其表达消失。Pax2参与胚胎肾脏各个发育阶段的调控。在肾脏发育的早期,Pax2通过激活未诱导的间充质表达GDNF而协调输尿管芽的出芽和定位,从而使肾脏发育开始,并调节随后的输尿管分支形成。Pax2-/-等位基因缺失的大鼠缺乏输尿管和生殖道,分析发现胚胎发育过程中Wolffian导管仅部分发育,而输尿管芽不能形成,其原因可能与Pax2缺失导致后肾间充质不能表达GNDF有关。在肾间充质细胞转化为肾单位上皮中Pax2也起关键作用,表现为促使间充质的压缩和向上皮细胞的转化,对以后的内皮细胞、系膜细胞的发育也有引导作用。Pax2基因突变发育过程中肾囊泡也不能形成,即间充质-上皮化受阻。目前研究认为Pax2可能是通过Pax2-Eya1-Six2轴起到对肾脏发育的调节作用(图1-3)。基因敲除实验发现Eya1-/-和Hoxa11-/-突变大鼠Pax2不能充分激活GDNF的表达,提示后肾间充质的诱导过程需要不同的转录因子的联合作用。

图1-3 输尿管芽和后肾间充质交互诱导的
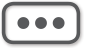
Eya基因可以编码含有Eya域的具有转激活活性的蛋白质,Eya1在胚胎发育中表达于后肾间充质,但不表达于输尿管芽及其衍生物。Eya1参与诱导间充质GDNF的表达及间充质-上皮转分化。Eya1-/-大鼠Pax2正常表达,而Six2和GDNF不能检测到,提示Pax2可能为Eya1的上游调控基因,而Six2和GDNF为Eya1的下游靶位。在人类单纯Eya1基因缺乏可导致支气管耳肾综合征和支气管眼综合征。
Six2为一个转录因子,含有Six型的同源域。Eya1和Six2直接相互作用,协同诱导对启动子的激活。但目前尚缺乏Six2基因敲除的实验模型。
Hoxa11和Foxc1(Mf1)参与Pax2-Eya1-Six2调节途径。两者胚胎发育中表达于后肾间充质,但不表达于输尿管芽及其衍生物。Hox基因属于同源盒核转录因子,含有4个相似的基因簇(HoxA-D)Hoxa11含有多对等位基因,Six2的表达水平依赖于功能性Hoxa11等位基因的数目,其中Hoxa11三对等位基因缺失的大鼠输尿管芽不能形成而导致无肾畸形,原位杂交显示Wt1、Pax2、Eya1正常表达,而Six2和GDNF缺如,提示Hoxa11位于Six2的上游。Foxc1属于叉头/翼螺旋转录基因家族,该家族含有一个进化中保守的DNA连接域,似乎直接参与Pax2-Eya1-Six2调节通路,基因敲除实验显示该家族在胚胎发育中起着重要作用,尤其在调节细胞增殖、细胞归属、细胞的分化方面。Foxc1功能基因缺乏可形成重复肾和输尿管畸形,额外从导管形成的输尿管位于正常输尿管之前,但不与膀胱连接。其原因可能是由于Eya1及GDNF的表达部位向前扩展,提示Foxc1可以抑制Eya1的表达,既而负性调节GDNF的表达。
3.Wt1和SaLL1的调节作用
Wt1基因与胚胎肾发育有关,它是一个转录调控因子。该基因编码的Wt1蛋白。其表达在时间和空间上受到严格的调控。Wt1在诱导前的后肾间充质以相对低的水平表达,随后在压缩间充质、肾囊泡、comma小体、S小体近端形成足细胞的部分高表达,成熟肾单位仅在足细胞表达,Bowan囊也有低水平的表达。Wt1参与肾脏发育各个阶段的调节,在肾脏发育的早期Wt1作为输尿管芽形成的诱导信号,同时亦为间充质细胞接受输尿管芽反馈信号的受体而维持间充质的存活。Wt1-/-大鼠后肾间充质可以形成,但输尿管芽不能从Wolffian导管发出,缺乏诱导信号的后肾间充质很快凋亡,因而后肾不能形成。在间充质上皮化过程中,Wt1作为上皮特异性蛋白的激活子,激活E钙粘连蛋白、Ⅳ胶原在上皮细胞的表达。有研究认为Wt1蛋白能抑制某些细胞增殖因子如早期生长反应因子Ⅰ(EGRⅠ)、类胰岛素生长因子Ⅱ(IGFⅡ)的转录,而促进某些与细胞分化有关的基因表达。在原位杂交中发现,在后肾胚基细胞向上皮细胞分化的过程中有Wt1mRNA的高表达,成熟上皮细胞中不再表达Wt1mRNA,表明Wt1基因是一个分化因子基因。其表达的Wt1蛋白可能是促进后肾胚基细胞向上皮细胞分化的调控因子。在胚胎肾组织分化完成之后,Wt1基因在细胞核的表达即被关闭,Wt1蛋白作为促分化因子的功能停止,但在胎儿后期肾脏的发育中Wt1基因仍然起作用,可能是促使肾小管发育成熟、功能完善的因素。
胚胎肾分化时期胚基细胞Wt1的表达发生障碍,可导致Wilm肿瘤、Denys-Drash综合征、Frasier综合征、孤立的弥漫性系膜硬化(IDMS)和特发性的持续性肾病综合征,肾病理上显示足细胞呈立方形,且足突形成严重受损,提示Wt1为足细胞分化的重要调控因子。进一步的研究发现Wt1在体外可以直接激活podocalyxin基因,而podocalyxin编码足细胞特异的蛋白。
SaLL1含有10个锌指域,在后肾发育过程中主要表达于环绕输尿管芽的间充质,在人类SaLL1杂合子突变导致Townes-Brocks综合征,表现为耳发育不良、多指畸形、肛门闭锁及肾脏心脏畸形。对SaLL1-/-大鼠后肾发育的研究显示输尿管芽可以形成,但既不能侵入间充质,也不能生长和形成分支,缺乏交互诱导信号,从而导致了输尿管芽和后肾间充质的凋亡。共培养实验显示SaLL1可以吸引输尿管芽,但基因分析显示其并不直接调节Pax2、Eya1、Wt1 Eya1及GDNF的表达,提示在Pax2-Eya1-Six2-和Wt1途径外可能还存在着其他的调节途径。
4.GDNF-Ret信号系统
以上调节途径对肾脏分支形成的调节均涉及对GDNF-Ret的调节。GDNFRet系统形成的信号传导复合体是输尿管芽形成和分支发育的基本调节子,在肾脏的分支形成中起着重要作用。GDNF或Ret基因失活均可使导致输尿管芽形成及分支障碍,导致肾脏不能发育或发育不良。GDNF是后肾间充质分泌的一种肽类生长因子,属于TGF-β超家族,表达于环绕输尿管芽的间充质,为Ret的配子,neurturin亦为Ret的另一配子。Ret为一种受体酪氨酸激酶,GFRα-1和GFRα-2为其共受体,表达仅限于输尿管芽顶端部位,调节输尿管芽的分支和生长。Ret表达的空间限制性对正常肾脏分支形成具有重要意义。
5.基质细胞表达分子的调节作用
输尿管芽和后肾间充质的分化发育不仅需要两者之间的相互作用,而且也需要与邻近基质细胞的相互作用。基质细胞在肾脏发育中的调节作用近年来渐渐引起重视。多种基质细胞因子参与输尿管芽和后肾间充质的分化发育,研究较多的是Foxd11(BF2)和维A酸的核受体RAR。
Foxd11(BF2)属于叉头/翼螺旋转录因子家族,是基质细胞特异性的转录因子,其确切作用目前尚不清楚。Foxd11(BF2)选择性地表达于压缩间充质细胞和分化中的肾单位周围的基质细胞,低水平的表达于环绕髓质输尿管芽分支的基质细胞。Foxd11删除导致基质细胞分化异常、肾脏皮质/髓质带缺乏、皮质发育不全和小肾畸形,进一步的分析发现压缩间充质细胞大量存在,而S小体、comma小体数目明显减少,Ret异常表达于整个输尿管芽,而导致肾发育不良,输尿管芽分支数量减少。以上研究提示基质细胞参与压缩间充质细胞向上皮细胞的转化和输尿管芽细胞的分化。
维生素A缺乏以及其代谢产物维A酸的核受体RAR突变的大鼠表现出的肾脏发育畸形与Ret-/-突变导致的相似,推测维A酸在肾发育中重要的作用之一是维持Ret在输尿管芽顶端的表达。RAR包括两个成员Rara、Rarb2。Rara在整个肾脏发育期以低水平表达,而Rarb2选择性表达于基质细胞。视黄醛脱氢酶Rald2是维A酸合成所必需的酶,定位于皮质基质,维生素A借助于基质细胞调节Ret在输尿管芽的表达。Rald2失活和RAR突变均可导致Ret表达下调,使分支形成受阻,同时基质细胞发育异常,大量积聚于肾包膜下。目前这一推测已被RAR突变的实验模型所证实。
基质细胞分泌的多种细胞因子也参与分支形成的调节。成纤维细胞生长因子FGFs是由基质细胞分泌的一类生长因子,研究显示FGFs参与对内外集合系统形成的调控。FGF-7、FGF-10基因缺失的大鼠显示髓质发育障碍,表现为肾乳头发育不良,Henle袢及髓质集合管数目的减少。FGF-7调节输尿管芽生长的范围,其受体为表达于输尿管芽和集合管系统的高黏附性的FGF-R-2b。FGF-7-/-的小鼠导致小肾畸形,FGF-10为FGF-R-2b受体的另一个配子,调节输尿管芽延长,提高FGF-10水平可导致输尿管芽极度延长。Foxd11(BF2)调节FGF-10的表达,定量分析显示Foxd11(BF2)-/-突变小鼠较Foxd11(BF2)+/-和野生型小鼠FGF-10水平为低,可以观察到集合管的截短,而出现明显的皮髓带缺陷。推测Foxd11(BF2)突变导致的肾脏畸形可能与FGF水平下降有关。
6.输尿管芽表达因子的调控作用
Emx2是一个同源盒基因,表达于Wolffian duct,输尿管芽及其衍生物,早期的上皮样结构的肾囊泡、comma小体。Emx2缺失突变的大鼠显示输尿管芽侵入间充质,但不能分支,不能诱导后肾间充质压缩,而很快凋亡,这与Pax2、Liml、Ret在输尿管芽的表达明显减少有关,进一步的研究显示在输尿管芽侵入之前GDNF的表达是正常的,但随后其表达在环绕输尿管芽的部位很快减少,Wnt4是间充质压缩产生的一种可溶性的分子,参与聚集细胞向小管的转化,也未表达于小管形成前的积聚物上,输尿管芽Emx2突变可能使其失去了对GDNF反应的能力,研究发现Emx2-/-突变的输尿管芽侵入后肾间充质之后其顶端Ret的表达丧失。此外,共培养实验显示Emx2可以调节输尿管芽细胞的分化,分化的细胞的产物可以产生诱导后肾间充质细胞上皮分化的信号。
Liml为含有Lim域的转录因子,编码核蛋白Liml,表达于输尿管芽分支、集合管、肾囊泡、comma小体、S小体及发育中的肾小管,Liml对头部器官的形成及在输尿管芽的生长和集合系统的形成中起重要作用,Liml-/-突变的大鼠肾脏不能形成。在哺乳动物,Liml可能参与上皮细胞的分化。
新近研究发现的Formin基因编码4个蛋白异构体,在肢芽和肾脏的发育中有重要作用,在肾脏发育中4个蛋白异构体均表达于输尿管芽,对输尿管芽的形成是必不可少的,Formin突变可导致肾脏不发育。Formin在肾脏发育中通过影响actin细胞骨架而影响输尿管芽形态发育中细胞的迁移。PKD-1基因编码一个基质蛋白受体polycystin-1,polycystin-1在调控actin细胞骨架、细胞极性、小管上皮细胞的终末分化中起重要作用。
肾单位发育的分子基础包括间充质细胞-上皮转分化形成肾小球肾小管上皮细胞、肾小球的血管化、肾单位的成熟等过程。
1.间充质细胞-上皮转分化
输尿管芽侵入间充质后,间充质在其顶端压缩,由非极性细胞转化为顶-基底侧极性的上皮细胞,开始了小管的形态发生。间充质细胞-上皮化过程中伴随着基质蛋白和细胞间黏附分子的变化。体外培养研究发现,与输尿管芽相联系的细胞首先聚集成上皮球,36小时后,这些聚集在一起的黏附细胞逐渐被一新形成的基底膜包绕,此时细胞停止表达后间充质特异的基质蛋白(胶原蛋白Ⅰ和Ⅲ),代之以上皮基质蛋白胶原蛋白Ⅳ,但仍能表达层粘连蛋白B亚基,并进一步表达层粘连蛋白A、a6整合素、E cadherin;72小时后,上皮细胞出现其特异性结构并表达肾特异性标志。完全极性化的上皮细胞高度表达E cadherin,此时均一的基质含有laminin,这些变化不仅是转化的特征,而且对上皮化和小管的发生是必需的。基质蛋白和细胞间黏附分子是极性化的最初调节分子,基质蛋白的表达可以确立细胞的基底侧并维持上皮细胞的活性。间充质-上皮转分化过程中基质蛋白、细胞间黏附分子、转录因子、多种细胞因子起着重要作用。
生长因子的调节作用:多种生长因子参与了肾脏发育的调节。输尿管芽源性的生长因子(由其分泌性的或其细胞表达的因子)对维持后间充质生存、避免其凋亡、促进其增殖和分化有重要作用。生长因子BMP S 、FGF、IL、EGF、NCAM具有间充质生长活性,其中作用最强的为LIF。LIF为IL-6家族成员之一,该家族其信号转导均通过表达于后肾间充质的共享受体gp130完成,进一步影响信号转导子和激活子STAT-3的转录。LIF对细胞的重构和小管发生有调节作用。细胞培养实验显示最初杂乱排列的后肾细胞在加入LIF后,E cadherin、层连蛋白α链、紧密连接蛋白ZO-I迅速表达,细胞重组为小链状的极性化的上皮细胞,继之极性化的上皮细胞形成小管。如果缺乏LIF则不能完成上皮化过程。间充质细胞亦可提供一些细胞因子,共同促进上皮转分化进程。目前认为HGF/SF及其酪氨酸激酶受体cmet在胚胎期间充质-上皮相互作用方面有重要意义。通常情况下,在胚胎发育过程中,HGF/SF主要表达在间充质细胞上,它可以促进上皮化细胞表达c-met。Woolf等研究表明,后肾间充质细胞同时表达HGF/SF和c-met,而“输尿管芽”只表达c-met,HGF/SF可以促进输尿管上皮的生长,也可以促进间质-上皮转分化。
转录因子的调节作用: 间充质细胞-上皮化过程中除上述已提及的Pax2、WT-1外,Wnt、Pod1、N-myc、HNF1α/LF-B1、Limx1b等在肾单位的发育中也起重要作用。
Wnt-4在早期胚胎发育过程中表达,Wnt-4以自分泌或旁分泌的形式作用于压缩的间充质细胞,促使其上皮化,协同Pax2、Pax8一起引导层粘连蛋白A、a6整合素、E cadherin基因同时表达,进而刺激间充质向上皮转分化。基因敲除实验显示Wnt-4-/-的大鼠输尿管芽诱导下间充质细胞可以形成压缩,但不能形成肾囊泡。Wnt-11表达于输尿管芽顶端,参与小管形成的诱导。
Pod1属于螺旋-袢-螺旋转录因子,为Wnt-4的下游因子,参与间充质细胞的上皮化。Pod1表达于环绕输尿管芽分支的压缩间充质、间质细胞和各阶段的足细胞,但不表达于其他上皮细胞,Pod1-/-的大鼠压缩间充质向上皮转化延迟且严重受损,小球数目减少,小管上皮细胞分化障碍,足细胞不能完成最终的分化,呈立方形,且足突数目少,肾小球形成阻滞于毛细血管袢阶段,毛细血管网密度明显下降,提示其与足细胞的分化和毛细血管的发育密切相关。
N-myc表达于上皮细胞前体细胞,参与调节上皮细胞生长但似乎不参与上皮细胞前体细胞的转化,上皮细胞转化过程中N-myc表达上调,基因敲除实验显示N-myc-/-大鼠体积小,但匀称。
HNF1α/LF-B1为一个二聚的同源域转录因子,选择性地表达于近端小管,调节近端小管细胞的分化,HNF1α-/-导致Fanconi综合征。
Limx1b为一个DNA连接蛋白,仅表达于足细胞,Limx1b-/-导致小球发育异常,足细胞发育障碍,缺乏毛细血管网,足细胞呈立方形,无足突和裂隙膜形成,进一步的分析发现足细胞不表达podocin,pro-α3(Ⅳ)胶原和pro-α4(Ⅳ)胶原链合成总量减少。
2.肾小球的血管发生和发育
肾小球的血管化即毛细血管的形成有赖于内皮细胞、足细胞、系膜细胞的协同作用。目前的研究认为在胚胎的成血管阶段,肾已经具备了所有的成血管前体细胞,包括内皮细胞、系膜细胞和肾素表达细胞。实验显示在完整的胚胎中,这些前体细胞也能形成肾的小动脉。
肾小球的血管化始于comma小体和S小体阶段。毛细血管的发育必须与足细胞的发育相一致。肾囊泡形成后在信号分子的作用下,招募成血管细胞进入肾小球,在S小体与输尿管芽连接相对的一极形成一个裂隙,是肾小球血管化的起始点。在血管裂隙内,迁徙的内皮细胞随着肾小球的生长经历有丝分裂,分化、增殖形成毛细血管,其基膜由内皮细胞和足细胞共同产细胞外基质成分组成,其后系膜细胞亦被招募入肾小球。系膜细胞有助于毛细血管袢的形成和固定。细胞因子及其受体在肾小球内皮细胞的分化、招募、有丝分裂、迁徙、毛细血管组装及稳固结构的形成中有重要作用。
(1)VEGF及其受体flt-1调节通路:
血管内皮生长因子(vascular endothelial growth factor,VEGF)及其受体酪氨酸激酶Flk1、Flt控制着早期及重要的胚胎血管发育。在肾脏,其表达服从于肾小球毛细血管的发育。VEGF表达于发育肾脏脉管系统周围的实质细胞,内源性和外源性的VEGF是一个内皮细胞形成原、丝裂原和趋化物,通过刺激肾脏本身固有的成血管细胞的增殖和分化而诱导血管形成。VEGF借助其受体Flk1、Flt1吸引内皮细胞向肾单位迁移形成肾小球的毛细血管,VEGF由近曲小管上皮细胞产生,形成了一个局部的吸引内皮细胞趋化的浓度梯度,而远曲小管上皮细胞则不吸引内皮细胞迁移。VEGF对内皮细胞的定向趋化梯度的产生是由Neuropilin-1、Neuropilin-2及其各自的配子-3A、semaphorins-3F所调节的,Neuropilin表达于内皮细胞,semaphorins表达于小管上皮细胞,VEGF和Neuropilin对肾脏血管空间结构的形成十分重要,但其具体的作用机制尚不清楚。
(2)Ang及其受体Tie调节通路:
Tie为内皮细胞受体酪氨酸激酶,包括Tie1和Tie2。Tie1的配子目前尚不明确,Tie2的配子有三个Ang-1(Angiopoietin-1,Ang-1)、Ang-2、Ang-3(在人类为Ang-1、Ang-2、Ang-4)。血管生成是多种正、负性调节因子直接或间接作用的结果,VEGF和Ang是两种主要的促血管生成因子。VEGF作用于血管形成早期,促进原始血管网形成;而Ang-1则作用于随后的血管改建、塑形,促进形成成熟、有空间结构的血管网。Ang与VEGF具有协同作用效应。Ang-2对血管生成的影响与局部微环境有关,当VEGF存在时,Ang-2可拮抗Ang-1促血管结构稳定的作用,消除血管基底膜和管周细胞对血管形成的限制,并增加内皮细胞对VEGF的敏感性,有利于血管出芽、生长,当VEGF缺乏时,Ang-2抑制Ang-1则有利于血管的消退。在肾脏发育中,E18~P3天,Ang-1表达于外皮质层的压缩间充质细胞、外髓层小管、肾小球、远曲小管。相反,Ang-2,E18~P1天仅表达于外髓层小管直部。E18~P1天,Tie2表达于毛细血管间质、动脉内皮细胞,至P3表达于肾小球、动脉内皮细胞、小管直部。虽然Tie 2/Ang的具体功能尚无具体的描述,但从其表达可以看出其在微血管发育中有重要作用。
(3)Eph受体和ephrin配体的调节:
Eph激酶组成了受体酪氨酸激酶的最大家族,目前已明确的Eph受体和ephrin配体共有14个成员。目前已获取的8种Eph受体家族的配体,依据与膜附着方式分为ephrinA和ephrinB两个亚组,ephrinA类配体靠糖基磷脂酰肌醇链(GPI linkage)锚定在细胞膜上,ephrinB类配体是单次跨膜蛋白,根据同源序列将Eph受体也分为两组:EphA和EphB受体。虽然ephrin配体与Eph受体可以混杂结合,但仍具有一些优先选择性。通常ephrinA型配体优先与EphA型受体结合,而ephrinB型配体则优先与EphB型受体结合。Eph受体和ephrin配体家族中,不同成员间具有剂量互补和功能重叠,但各自参与特定的组织和器官的许多的发育进程。Eph/ephrin家族在发育肾的表达可能有助于内皮细胞向血管裂隙的定向迁移。ephrinB2最初表达于脏层上皮细胞,继之表达于发育中的肾小球内皮细胞,当内皮细胞前体细胞与ephrinB2阳性的足细胞前体细胞同位时,内皮细胞开始招募系膜细胞形成毛细血管支持结构,这种模式持续至足细胞成熟,ephrinB2关闭。ephrinB2这种在发育肾足细胞和内皮细胞的次序表达是为内皮细胞和系膜细胞前体细胞的招募提供一个位点。ephrinB2/EphB2也表达于邻近血管的间充质上,提示Eph家族蛋白也具有调节间充质与内皮细胞之间的相互作用。在成年肾脏ephrinB2表达于动脉和肾小球毛细血管内皮细胞和集合管上皮细胞,提示其可能也参与成熟内皮细胞和肾集合管上皮细胞的维持,但目前其作用机制尚不明确。EphB4表达局限于静脉内皮细胞,不参与肾小球毛细血管的形成。
3.肾单位的成熟
肾单位的成熟是指完全分化的上皮细胞为适应其排泄最终代谢产物、毒物维持水电解质平衡的功能而具有的较之胚胎期上皮细胞更为复杂的膜形态,包括基底侧的绒毛、膜顶端的微绒毛以及大量表达的转运蛋白等。生后肾脏的成熟需要一个较长的时期,几乎在各种程度上新生儿的转运功能均低于成人。
发育肾的研究是近年来肾脏病领域的一个研究热点,综上所述,肾脏的发育是一个由复杂的分子信号调控的过程,阐明肾脏发育过程中复杂的分子信号转导机制有助于揭示先天性肾脏发育不良的机制,同时对发育肾的研究也有助于理解后天性肾脏疾病发生进展的病理生理机制,从而为肾脏病的诊治提供新的思路。
(白海涛)